История медицинских открытий | ФГБУ «НМИЦ эндокринологии» Минздрава России
ИСТОРИЯ МЕДИЦИНЫ:
ОСНОВНЫЕ ВЕХИ И ВЕЛИКИЕ ОТКРЫТИЯ
По материалам телеканала Дискавери
(«Discovery Channel»)
Открытия в медицине преобразили мир. Они изменили ход истории, сохранив несчётное количество жизней, раздвинув границы наших познаний до рубежей, на которых мы стоим сегодня, готовые к новым великим открытиям.
Анатомия человека
В Древней Греции лечение болезней основывалось скорее на философии, чем на истинном понимании анатомии человека. Хирургическое вмешательство было редкостью, а препарирование трупов ещё не практиковалось. В результате врачи практически не имели сведений о внутреннем устройстве человека. Лишь в эпоху Ренессанса анатомия зародилась как наука.
Бельгийский врач Андреас Везалий шокировал многих, когда решил изучать анатомию, вскрывая трупы. Материал для исследований приходилось добывать под покровом ночи.
Кровообращение
Сердце человека – мышца размером с кулак. Оно сокращается более ста тысяч раз в день, за семьдесят лет – это два с лишним миллиарда сердцебиений. Сердце перекачивает 23 литра крови в минуту. Кровь течёт по телу, проходя через сложную систему артерий и вен. Если все кровеносные сосуды в человеческом теле вытянуть в одну линию, то получится 96 тысяч километров, что в два с лишним раза больше окружности Земли. До начала 17 века процесс кровообращения представляли неверно. Преобладала теория, согласно которой кровь приливала к сердцу через поры в мягких тканях тела. Среди приверженцев этой теории был и английский врач Уильям Гарвей. Работа сердца завораживала его, но чем больше он наблюдал биение сердца у животных, тем сильнее понимал, что общепринятая теория кровообращения попросту неверна. Он недвусмысленно пишет: «…Я подумал, не может ли кровь двигаться, словно по кругу?». И первая же фраза в следующем абзаце: «Впоследствии я выяснил, что так оно и есть…». Проводя вскрытия, Гарвей обнаружил, что у сердца есть однонаправленные клапаны, позволяющие крови течь лишь в одном направлении.
Оно сокращается более ста тысяч раз в день, за семьдесят лет – это два с лишним миллиарда сердцебиений. Сердце перекачивает 23 литра крови в минуту. Кровь течёт по телу, проходя через сложную систему артерий и вен. Если все кровеносные сосуды в человеческом теле вытянуть в одну линию, то получится 96 тысяч километров, что в два с лишним раза больше окружности Земли. До начала 17 века процесс кровообращения представляли неверно. Преобладала теория, согласно которой кровь приливала к сердцу через поры в мягких тканях тела. Среди приверженцев этой теории был и английский врач Уильям Гарвей. Работа сердца завораживала его, но чем больше он наблюдал биение сердца у животных, тем сильнее понимал, что общепринятая теория кровообращения попросту неверна. Он недвусмысленно пишет: «…Я подумал, не может ли кровь двигаться, словно по кругу?». И первая же фраза в следующем абзаце: «Впоследствии я выяснил, что так оно и есть…». Проводя вскрытия, Гарвей обнаружил, что у сердца есть однонаправленные клапаны, позволяющие крови течь лишь в одном направлении.
Открытие Гарвея серьёзно продвинуло вперёд анатомию и хирургию, а многим попросту спасло жизнь. Во всём мире в операционных применяют хирургические зажимы, блокирующие течение крови и сохраняющие систему кровообращения пациента в неприкосновенности. И каждый из них — напоминание о великом открытии Уильяма Гарвея.
Группы крови
Другое великое открытие, связанное с кровью, было сделано в Вене в 1900 году.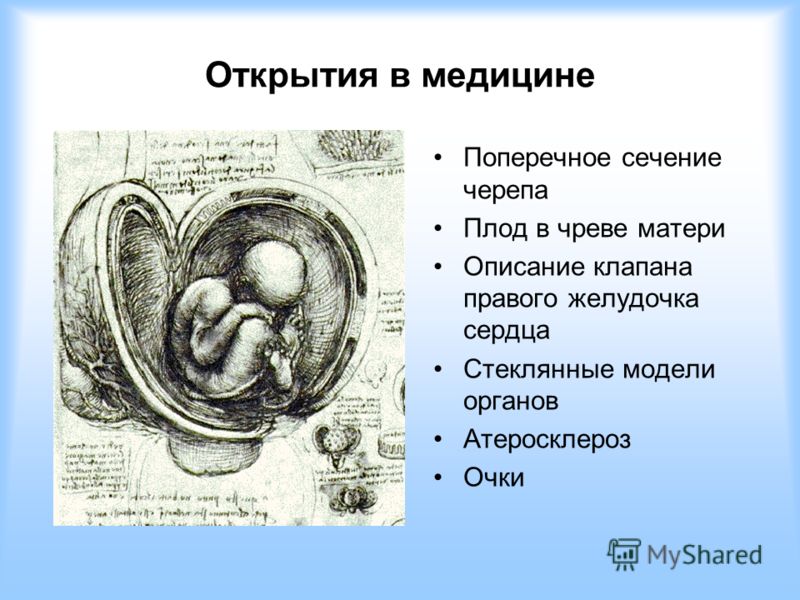 Всю Европу переполнял энтузиазм по поводу переливания крови. Сначала прошли заявления, что лечебный эффект поразительный, а затем, через несколько месяцев, сообщения о погибших. Почему иногда переливание проходило удачно, а иногда — нет? Австрийский врач Карл Ландштейнер был полон решимости найти ответ. Он смешал образцы крови от разных доноров и изучил результаты.
Всю Европу переполнял энтузиазм по поводу переливания крови. Сначала прошли заявления, что лечебный эффект поразительный, а затем, через несколько месяцев, сообщения о погибших. Почему иногда переливание проходило удачно, а иногда — нет? Австрийский врач Карл Ландштейнер был полон решимости найти ответ. Он смешал образцы крови от разных доноров и изучил результаты.
В некоторых случаях кровь смешалась удачно, зато в других — свернулась и стала вязкой. При ближайшем рассмотрении Ландштейнер обнаружил, что кровь сворачивается, когда особые белки в крови реципиента, так называемые антитела, вступают в реакцию с другими белками в эритроцитах донора – антигенами. Для Ландштейнера это был поворотный момент. Он осознал, что не вся человеческая кровь одинакова. Оказалось, что кровь можно чётко разделить на 4 группы, которым он дал обозначения: А, Б, АБ и нулевая. Выяснилось, что переливание крови проходит успешно лишь в том случае, если человеку переливают кровь той же группы. Открытие Ландштейнера тут же отразилось на медицинской практике.
Анестезия
Хотя первые великие открытия в области анатомии и позволили врачам спасти множество жизней, они никак не могли облегчить боль. Без анестезии операции были кошмаром наяву. Пациентов держали или привязывали к столу, хирурги старались работать как можно быстрее. В 1811 году одна женщина писала: «Когда ужасная сталь вонзилась в меня, рассекая вены, артерии, плоть, нервы, меня уже не нужно было просить не вмешиваться. Я издала вопль и кричала, пока всё не закончилось. Так невыносима была мука». Хирургия была последним средством, многие предпочитали умереть, чем лечь под нож хирурга. На протяжении веков для облегчения боли во время операций использовались подручные средства некоторые из них, например, опиум или экстракт мандрагоры, были наркотиками.
Пациенту, которому предстояло удалить опухоль на шее, дали эфир. Мортон подождал, хирург произвёл первый надрез. Поразительно, но пациент не закричал. После операции пациент сообщил, что всё это время ничего не чувствовал.
 Весть об открытии разнеслась по всему миру. Оперировать без боли можно, теперь есть анестезия. Но, несмотря на открытие, многие отказывались воспользоваться анестезией. Согласно некоторым вероучениям, боль надо терпеть, а не облегчать, особенно родовые муки. Но здесь свое слово сказала королева Виктория. В 1853 году она рожала принца Леопольда. По её просьбе ей дали хлороформ. Оказалось, что он облегчает муки деторождения. После этого женщины стали говорить: «Я тоже приму хлороформ, ведь если им не брезгует королева, то и мне не зазорно».
Весть об открытии разнеслась по всему миру. Оперировать без боли можно, теперь есть анестезия. Но, несмотря на открытие, многие отказывались воспользоваться анестезией. Согласно некоторым вероучениям, боль надо терпеть, а не облегчать, особенно родовые муки. Но здесь свое слово сказала королева Виктория. В 1853 году она рожала принца Леопольда. По её просьбе ей дали хлороформ. Оказалось, что он облегчает муки деторождения. После этого женщины стали говорить: «Я тоже приму хлороформ, ведь если им не брезгует королева, то и мне не зазорно». Рентгеновские лучи
Невозможно представить себе жизнь без следующего великого открытия. Вообразите, что мы не знаем, где оперировать больного, или какая именно кость сломана, где застряла пуля и какая может быть патология. Способность заглянуть внутрь человека, не разрезая его, стала поворотным моментом в истории медицины. В конце 19 века люди использовали электричество, толком не понимая, что это такое. В 1895 году немецкий физик Вильгельм Рентген экспериментировал с электронно-лучевой трубкой, стеклянным цилиндром с сильно разреженным воздухом внутри.
Утверждают, что жена сказала: «Я видела свою смерть». Ведь в те времена нельзя было увидеть скелет человека, если он не умер.
 Сама мысль о том, чтобы заснять внутреннее строение живого человека, просто не укладывалась в голове. Словно распахнулась тайная дверь, а за ней открылась целая вселенная. Рентген открыл новую, мощную технологию, которая произвела переворот в области диагностики. Открытие рентгеновского излучения — это единственное в истории науки открытие, сделанное непреднамеренно, совершенно случайное. Едва оно было сделано, мир тотчас же принял его на вооружение безо всяких дебатов. За неделю-другую наш мир преобразился. На открытие рентгена опираются многие из самых современных и мощных технологий, от компьютерной томографии до рентгенографического телескопа, улавливающего рентгеновские лучи из глубин космоса. И всё это – из-за открытия, сделанного случайно.
Сама мысль о том, чтобы заснять внутреннее строение живого человека, просто не укладывалась в голове. Словно распахнулась тайная дверь, а за ней открылась целая вселенная. Рентген открыл новую, мощную технологию, которая произвела переворот в области диагностики. Открытие рентгеновского излучения — это единственное в истории науки открытие, сделанное непреднамеренно, совершенно случайное. Едва оно было сделано, мир тотчас же принял его на вооружение безо всяких дебатов. За неделю-другую наш мир преобразился. На открытие рентгена опираются многие из самых современных и мощных технологий, от компьютерной томографии до рентгенографического телескопа, улавливающего рентгеновские лучи из глубин космоса. И всё это – из-за открытия, сделанного случайно.Теория микробного происхождения болезней
Одни открытия, например, рентгеновские лучи, совершаются случайно, над другими долго и упорно работают различные учёные. Так было и в 1846 год. Вена. Воплощение красоты и культуры, но в венской городской больнице витает призрак смерти. Многие из находившихся здесь рожениц умирали. Причина – родильная горячка, инфекция матки. Когда доктор Игнац Земмельвейс начал работать в этой больнице, он был встревожен масштабом бедствия и озадачен странной несообразностью: там было два отделения.
Многие из находившихся здесь рожениц умирали. Причина – родильная горячка, инфекция матки. Когда доктор Игнац Земмельвейс начал работать в этой больнице, он был встревожен масштабом бедствия и озадачен странной несообразностью: там было два отделения.
В одном роды принимали врачи, а в другом роды у матерей принимали акушерки. Земмельвейс обнаружил, что в том отделении, где роды принимали врачи, 7% рожениц умерло от так называемой родильной горячки. А в отделении, где работали акушерки, от родильной горячки скончались лишь 2%. Это его удивило, ведь у врачей подготовка гораздо лучше. Земмельвейс решил выяснить, в чём же причина. Он заметил, что одним из главных различий в работе врачей и акушерок было то, что врачи проводили вскрытие умерших рожениц. Затем они шли принимать роды или осматривать матерей, даже не вымыв рук. Земмельвейс задумался, не переносят ли врачи на своих руках некие невидимые частички, которые затем передаются пациенткам и влекут за собой смерть. Чтобы выяснить это, он провёл опыт. Он решил проследить, чтобы все студенты медики в обязательном порядке мыли руки в растворе хлорной извести. И количество летальных исходов тут же упало до 1%, ниже, чем у акушерок. Благодаря этому эксперименту, Земмельвейс осознал, что инфекционные заболевания, в данном случае, родильная горячка, имеют лишь одну причину и если ее исключить, болезнь не возникнет. Но в 1846 году никто не усматривал связи между бактериями и инфекцией. Идеи Земмельвейса не приняли всерьёз.
Он решил проследить, чтобы все студенты медики в обязательном порядке мыли руки в растворе хлорной извести. И количество летальных исходов тут же упало до 1%, ниже, чем у акушерок. Благодаря этому эксперименту, Земмельвейс осознал, что инфекционные заболевания, в данном случае, родильная горячка, имеют лишь одну причину и если ее исключить, болезнь не возникнет. Но в 1846 году никто не усматривал связи между бактериями и инфекцией. Идеи Земмельвейса не приняли всерьёз.
Прошло ещё целых 10 лет, прежде чем на микроорганизмы обратил внимание другой учёный. Его звали Луи Пастер.Трое из пяти детей Пастера умерли от брюшного тифа, что отчасти объясняет, почему он так упорно искал причину инфекционных болезней. На верный след Пастера вывела его работа для винодельческой и пивоваренной промышленности. Пастер пытался выяснить, почему лишь малая часть вина, производимого в его стране, портится. Он обнаружил, что в прокисшем вине есть особые микроорганизмы, микробы, и именно они заставляют вино скисать. Но путём простого нагрева, как показал Пастер, микробы можно убить, и вино будет спасено. Так родилась пастеризация. Поэтому, когда потребовалось найти причину инфекционных заболеваний, Пастер знал, где её искать. Это микробы, сказал он, вызывают определённые болезни, и доказал это, проведя серию экспериментов, из которых родилось великое открытие – теория микробного развития организмов. Её суть состоит в том, что определённые микроорганизмы вызывают определённую болезнь у любого.
Но путём простого нагрева, как показал Пастер, микробы можно убить, и вино будет спасено. Так родилась пастеризация. Поэтому, когда потребовалось найти причину инфекционных заболеваний, Пастер знал, где её искать. Это микробы, сказал он, вызывают определённые болезни, и доказал это, проведя серию экспериментов, из которых родилось великое открытие – теория микробного развития организмов. Её суть состоит в том, что определённые микроорганизмы вызывают определённую болезнь у любого.
Вакцинация
Следующее из великих открытий было сделано в 18 веке, когда от оспы во всём мире умерло около 40 млн. человек. Врачи не могли найти ни причины возникновения болезни, ни средства от неё. Но в одной английской деревушке разговоры о том, что часть местных жителей не восприимчивы к оспе, привлекли внимание местного врача по имени Эдвард Дженнер.
Ходили слухи, что работницы молочных ферм не болеют оспой, потому что уже перенесли коровью оспу, родственную, но более лёгкую болезнь, поражавшую скот. У больных коровьей оспой поднималась температура и на руках возникали язвочки. Дженнер изучил этот феномен и задумался, может быть, гной из этих язвочек каким-то образом защищает организм от оспы? 14 мая 1796 года во время вспышки эпидемии оспы, он решил проверить свою теорию. Дженнер взял жидкость из язвочки на руке доярки, больной коровьей оспой. Затем, он посетил другую семью; там он ввёл здоровому восьмилетнему мальчику вирус коровьей оспы. В последующие дни у мальчика был лёгкий жар, и появилось несколько оспенных пузырьков. Затем он поправился. Через шесть недель Дженнер вернулся. На этот раз он привил мальчику оспу и стал ждать, чем обернётся эксперимент – победой или провалом. Через несколько дней Дженнер получил ответ – мальчик был совершенно здоров и невосприимчив к оспе.
У больных коровьей оспой поднималась температура и на руках возникали язвочки. Дженнер изучил этот феномен и задумался, может быть, гной из этих язвочек каким-то образом защищает организм от оспы? 14 мая 1796 года во время вспышки эпидемии оспы, он решил проверить свою теорию. Дженнер взял жидкость из язвочки на руке доярки, больной коровьей оспой. Затем, он посетил другую семью; там он ввёл здоровому восьмилетнему мальчику вирус коровьей оспы. В последующие дни у мальчика был лёгкий жар, и появилось несколько оспенных пузырьков. Затем он поправился. Через шесть недель Дженнер вернулся. На этот раз он привил мальчику оспу и стал ждать, чем обернётся эксперимент – победой или провалом. Через несколько дней Дженнер получил ответ – мальчик был совершенно здоров и невосприимчив к оспе.
Изобретение вакцинации от оспы произвело революцию в медицине. Это была первая попытка вмешаться в течение болезни, предотвратив её заранее. Впервые средства, изготовленные человеком, активно использовались, чтобы предотвратить болезнь ещё до её появления.
Через 50 лет после открытия Дженнера, Луи Пастер развил идею вакцинации, разработав вакцину от бешенства у людей и от сибирской язвы у овец. А в 20 веке Джонас Солк и Альберт Сейбин , независимо друг от друга, создали вакцину от полиомиелита.
Витамины
Следующее открытие состоялось трудами учёных, многие годы независимо друг от друга бившихся над одной и той же проблемой.
На протяжении всей истории цинга была тяжёлым заболеванием, вызывавшим у моряков поражения кожи и кровотечения. Наконец, в 1747 году корабельный хирург шотландец Джеймс Линд нашёл от неё средство. Он обнаружил, что цингу можно предотвратить, включив в рацион матросов цитрусовые.
Другим частым заболеванием у моряков была бери-бери, болезнь, поражавшая нервы, сердце и пищеварительный тракт. В конце 19 века голландский врач Христиан Эйкман определил, что болезнь обусловлена употреблением в пищу белого шлифованного риса, вместо бурого нешлифованного.
Хотя оба этих открытия указывали на связь заболеваний с питанием и его недостатками, в чём заключалась эта связь смог выяснить лишь английский биохимик Фредерик Хопкинс. Он предположил, что организму необходимы вещества, которые есть только в определённых продуктах. Чтобы доказать свою гипотезу, Хопкинс провёл серию экспериментов. Он давал мышам искусственное питание, состоящее исключительно из чистых белков, жиров, углеводов и солей. Мыши ослабли и перестали расти. Но после небольшого количества молока, мыши снова поправились. Хопкинс открыл, как он выразился, «незаменимый фактор питания», который позже назвали витаминами.
Он предположил, что организму необходимы вещества, которые есть только в определённых продуктах. Чтобы доказать свою гипотезу, Хопкинс провёл серию экспериментов. Он давал мышам искусственное питание, состоящее исключительно из чистых белков, жиров, углеводов и солей. Мыши ослабли и перестали расти. Но после небольшого количества молока, мыши снова поправились. Хопкинс открыл, как он выразился, «незаменимый фактор питания», который позже назвали витаминами.
Оказалось, что бери-бери связана с недостатком тиамина, витамина В1, которого нет в шлифованном рисе, но много в натуральном. А цитрусовые предотвращают цингу, потому что содержат аскорбиновую кислоту, витами С.
Открытие Хопкинса стало определяющим шагом в понимании важности правильного питания. От витаминов зависит множество функций организма – от борьбы с инфекциями до регулирования обмена веществ. Без них трудно представить себе жизнь, как и без следующего великого открытия.
Пенициллин
После Первой Мировой войны, унесшей свыше 10 млн. жизней, поиски безопасных методов отражения бактериальной агрессии усилились. Ведь многие умерли не на полях сражений, а от инфицированных ран. В исследованиях участвовал и шотландский врач Александр Флеминг. Изучая бактерии стафилококки, Флеминг заметил, что в центре лабораторной чаши растёт нечто необычное — плесень. Он увидел, что вокруг плесени бактерии погибли. Это заставило его предположить, что она выделяет вещество, губительное для бактерий. Это вещество он назвал пенициллином. Следующие несколько лет Флеминг пытался выделить пенициллин и применить его в лечении инфекций, но неудачно, и, в конце концов, сдался. Однако результаты его трудов оказались неоценимыми.
жизней, поиски безопасных методов отражения бактериальной агрессии усилились. Ведь многие умерли не на полях сражений, а от инфицированных ран. В исследованиях участвовал и шотландский врач Александр Флеминг. Изучая бактерии стафилококки, Флеминг заметил, что в центре лабораторной чаши растёт нечто необычное — плесень. Он увидел, что вокруг плесени бактерии погибли. Это заставило его предположить, что она выделяет вещество, губительное для бактерий. Это вещество он назвал пенициллином. Следующие несколько лет Флеминг пытался выделить пенициллин и применить его в лечении инфекций, но неудачно, и, в конце концов, сдался. Однако результаты его трудов оказались неоценимыми.
В 1935 году сотрудники Оксфордского университета Хоуард Флори и Эрнст Чейн наткнулись на отчёт о любопытных, но незаконченных экспериментах Флеминга, и решили попытать счастья. Этим учёным удалось выделить пенициллин в чистом виде. И в 1940-ом году они провели его испытание. Восьми мышам была введена смертельная доза бактерий стрептококков. Затем, четырём из них ввели пенициллин. Через несколько часов результаты были налицо. Все четыре, не получившие пенициллин мыши умерли, но три из четверых получивших его — выжили.
Затем, четырём из них ввели пенициллин. Через несколько часов результаты были налицо. Все четыре, не получившие пенициллин мыши умерли, но три из четверых получивших его — выжили.
Так, благодаря Флемингу, Флори и Чейну, мир получил первый антибиотик. Это лекарство стало настоящим чудом. Оно лечило от стольких недугов, которые причиняли много боли и страданий: острый фарингит, ревматизм, скарлатина, сифилис и гонорея… Сегодня мы уже совсем забыли, что от этих болезней можно умереть.
Сульфидные препараты
Следующее великое открытие подоспело во время Второй Мировой войны. Оно избавило от дизентерии американских солдат, сражавшихся в тихоокеанском бассейне. А затем привело к революции в химиотерапевтическом лечении бактериальных инфекций.
Случилось всё это благодаря патологу по имени Герхард Домагк. В 1932 году он изучал возможности применения в медицине некоторых новых химических красителей. Работая с недавно синтезированным красителем под названием пронтозил, Домагк ввёл его нескольким лабораторным мышам, заражённым бактериями стрептококками. Как и ожидал Домагк, краситель обволок бактерии, но бактерии выжили. Казалось, краситель недостаточно токсичен. Затем случилось нечто поразительное: хотя краситель и не убил бактерии, он остановил их рост, распространение инфекции прекратилось и мыши выздоровели. Когда Домагк впервые испытал пронтозил на людях — неизвестно. Однако новое лекарство стяжало славу после того, как спасло жизнь мальчику, серьёзно больному стафилококком. Пациентом был Франклин Рузвельт-младший, сын президента Соединённых Штатов. Открытие Домагка мгновенно стало сенсацией. Поскольку пронтозил содержал сульфамидную молекулярную структуру, его назвали сульфамидным препаратом. Он стал первым в этой группе синтетических химических веществ, способных лечить и предотвращать бактериальные инфекции. Домагк открыл новое революционное направление в лечении болезней, использовании химиотерапевтических препаратов. Оно спасёт десятки тысяч человеческих жизней.
Как и ожидал Домагк, краситель обволок бактерии, но бактерии выжили. Казалось, краситель недостаточно токсичен. Затем случилось нечто поразительное: хотя краситель и не убил бактерии, он остановил их рост, распространение инфекции прекратилось и мыши выздоровели. Когда Домагк впервые испытал пронтозил на людях — неизвестно. Однако новое лекарство стяжало славу после того, как спасло жизнь мальчику, серьёзно больному стафилококком. Пациентом был Франклин Рузвельт-младший, сын президента Соединённых Штатов. Открытие Домагка мгновенно стало сенсацией. Поскольку пронтозил содержал сульфамидную молекулярную структуру, его назвали сульфамидным препаратом. Он стал первым в этой группе синтетических химических веществ, способных лечить и предотвращать бактериальные инфекции. Домагк открыл новое революционное направление в лечении болезней, использовании химиотерапевтических препаратов. Оно спасёт десятки тысяч человеческих жизней.
Инсулин
Следующее великое открытие помогло спасти жизнь миллионам больных диабетом во всём мире. Диабет — это недуг, нарушающий процесс усвоения организмом сахара, что может привести к слепоте, отказу почек, заболеваниям сердца и даже к смерти. Столетиями медики изучали диабет, безуспешно ища от него средства. Наконец, в конце 19 века, произошёл прорыв. Было установлено, что у больных диабетом есть общая черта — неизменно поражена группа клеток в поджелудочной железе — эти клетки выделяют гормон, контролирующий содержание сахара в крови. Гормон назвали инсулином. А в 1920 году — новый прорыв. Канадский хирург Фредерик Бантинг и студент Чарльз Бест изучали секрецию инсулина поджелудочной железы у собак. Повинуясь интуиции, Бантинг ввёл экстракт из вырабатывающих инсулин клеток здоровой собаки собаке, страдающей диабетом. Результаты были ошеломляющими. Через несколько часов уровень сахара в крови больного животного существенно понизился. Теперь внимание Бантинга и его помощников сосредоточилось на поисках животного, чей инсулин был бы схож с человеческим. Они нашли близкое соответствие в инсулине, взятом у зародышей коров, очистили его для безопасности эксперимента и в январе 1922 года провели первое клиническое испытание.
Диабет — это недуг, нарушающий процесс усвоения организмом сахара, что может привести к слепоте, отказу почек, заболеваниям сердца и даже к смерти. Столетиями медики изучали диабет, безуспешно ища от него средства. Наконец, в конце 19 века, произошёл прорыв. Было установлено, что у больных диабетом есть общая черта — неизменно поражена группа клеток в поджелудочной железе — эти клетки выделяют гормон, контролирующий содержание сахара в крови. Гормон назвали инсулином. А в 1920 году — новый прорыв. Канадский хирург Фредерик Бантинг и студент Чарльз Бест изучали секрецию инсулина поджелудочной железы у собак. Повинуясь интуиции, Бантинг ввёл экстракт из вырабатывающих инсулин клеток здоровой собаки собаке, страдающей диабетом. Результаты были ошеломляющими. Через несколько часов уровень сахара в крови больного животного существенно понизился. Теперь внимание Бантинга и его помощников сосредоточилось на поисках животного, чей инсулин был бы схож с человеческим. Они нашли близкое соответствие в инсулине, взятом у зародышей коров, очистили его для безопасности эксперимента и в январе 1922 года провели первое клиническое испытание. Бантинг ввёл инсулин 14-летнему мальчику, умиравшему от диабета. И тот стремительно пошёл на поправку. На сколько важно открытие Бантинга? Спросите об этом 15 миллионов американцев, которые ежедневно получают инсулин, от которого зависит их жизнь.
Бантинг ввёл инсулин 14-летнему мальчику, умиравшему от диабета. И тот стремительно пошёл на поправку. На сколько важно открытие Бантинга? Спросите об этом 15 миллионов американцев, которые ежедневно получают инсулин, от которого зависит их жизнь.
Генетическая природа рака
Рак — вторая по летальности болезнь в Америке. Интенсивные исследования его возникновения и развития привели к замечательным научным свершениям, но, пожалуй, самым важным из них стало следующее открытие. Нобелевские лауреаты, исследователи рака Майкл Бишоп и Харольд Вармус, объединили усилия в исследовании рака в 70-х годах 20 века. В то время доминировало несколько теорий о причине этого заболевания. Злокачественная клетка очень непроста. Она способна не только делиться, но и вторгаться. Это клетка с высокоразвитыми возможностями. В одной из теорий рассматривался вирус саркомы Рауса, вызывающий рак у кур. Когда вирус нападает на клетку курицы, он вводит свой генетический материал в ДНК хозяина. Согласно гипотезе, ДНК вируса становится впоследствии агентом, вызывающим заболевание. По другой теории, при вводе вирусом своего генетического материала в клетку хозяина, гены, вызывающие рак, не активируются, а ждут, пока их не запустит внешнее воздействие, например, вредные химикаты, радиация или обычная вирусная инфекция. Эти вызывающие рак гены, так называемые онкогены, и стали объектом исследований Вармуса и Бишопа. Главный вопрос: содержит ли геном человека гены, являющиеся или способные стать онкогенами вроде тех, что содержатся в вирусе, вызывающем опухоли? Есть ли такой ген у кур, у других птиц, у млекопитающих, у человека? Бишоп и Вармус взяли меченную радиоактивную молекулу и использовали её в качестве зонда, чтобы выяснить, похож ли онкоген вируса саркомы Рауса на какой-нибудь нормальный ген в хромосомах курицы. Ответ утвердительный. Это было настоящее откровение. Вармус и Бишоп установили, что вызывающий рак ген уже содержится в ДНК здоровых клеток курицы и, что ещё важнее, они обнаружили его и в ДНК человека, доказав, что зародыш рака может явиться в любом из нас на клеточном уровне и ждать активации.
Согласно гипотезе, ДНК вируса становится впоследствии агентом, вызывающим заболевание. По другой теории, при вводе вирусом своего генетического материала в клетку хозяина, гены, вызывающие рак, не активируются, а ждут, пока их не запустит внешнее воздействие, например, вредные химикаты, радиация или обычная вирусная инфекция. Эти вызывающие рак гены, так называемые онкогены, и стали объектом исследований Вармуса и Бишопа. Главный вопрос: содержит ли геном человека гены, являющиеся или способные стать онкогенами вроде тех, что содержатся в вирусе, вызывающем опухоли? Есть ли такой ген у кур, у других птиц, у млекопитающих, у человека? Бишоп и Вармус взяли меченную радиоактивную молекулу и использовали её в качестве зонда, чтобы выяснить, похож ли онкоген вируса саркомы Рауса на какой-нибудь нормальный ген в хромосомах курицы. Ответ утвердительный. Это было настоящее откровение. Вармус и Бишоп установили, что вызывающий рак ген уже содержится в ДНК здоровых клеток курицы и, что ещё важнее, они обнаружили его и в ДНК человека, доказав, что зародыш рака может явиться в любом из нас на клеточном уровне и ждать активации.
Как может наш собственный ген, с которым мы прожили всю жизнь, вызвать рак? При делении клеток случаются ошибки и они чаще, если клетка угнетена космическим излучением, табачным дымом. Важно также помнить, что, когда клетка делится, ей надо скопировать 3 млрд. комплементарных пар ДНК. Всякий, кто хоть раз пытался печатать, знает, как это трудно. У нас есть механизмы, позволяющие замечать и исправлять ошибки, и всё же, при больших объёмах, пальцы промахиваются.
В чём же важность открытия? Раньше рак пытались осмыслить, исходя из различий между геном вируса и геном клетки, а теперь мы знаем, что совсем небольшое изменение в определённых генах наших клеток может превратить здоровую клетку, которая нормально растёт, делится и т.д., в злокачественную. И это стало первой ясной иллюстрацией истинного положения вещей.
Поиски данного гена — определяющий момент в современной диагностике и предсказании дальнейшего поведения раковой опухоли. Открытие дало чёткие цели специфическим видам терапии, которых раньше попросту не было.
Население Чикаго около 3 млн. человек.
ВИЧ
Столько же ежегодно умирают от СПИДа, одной из самых страшных эпидемий в новой истории. Первые признаки этого заболевания появились в начале 80-х годов прошлого века. В Америке стало расти число пациентов, умиравших от редких видов инфекций и рака. Анализ крови у жертв выявил крайне низкий уровень лейкоцитов — белых кровяных клеток, жизненно важных для иммунной системы человека. В 1982 году Центр контроля и предотвращения заболеваний дал болезни название СПИД — синдром приобретённого иммунодефицита. За дело взялись двое исследователей, Люк Монтанье из института Пастера в Париже и Роберт Галло из Национального института онкологии в Вашингтоне. Им обоим удалось сделать важнейшее открытие, которое выявило возбудителя СПИДа — ВИЧ, вирус иммунодефицита человека. В чём отличие вируса иммунодефицита человека от других вирусов, например, гриппа? Во-первых, этот вирус годами не выдаёт наличие болезни, в среднем, 7 лет. Вторая проблема весьма уникальна: например, СПИД наконец проявился, люди понимают, что больны и идут в клинику, а у них, мириад других инфекций, что именно стало причиной заболевания. Как это определить? В большинстве случаев вирус существует ради единственной цели: проникнуть в клетку-акцептор и размножиться. Обычно, он прикрепляется к клетке и выпускает в неё свою генетическую информацию. Это позволяет вирусу подчинить себе функции клетки, перенаправив их на производство новых особей вирусов. Затем эти особи нападают на другие клетки. Но ВИЧ — это не рядовой вирус. Он принадлежит к той категории вирусов, которых учёные называют ретровирусами. Что же в них необычного? Подобно тем классам вирусов, куда входят полиомиелит или грипп, ретровирусы — особые категории. Они уникальны тем, что их генетическая информация в виде рибонуклеиновой кислоты конвертируется в дезоксирибонуклеиновую кислоту (ДНК) и как раз то, что происходит с ДНК, и составляет нашу проблему: ДНК встраивается в наши гены, ДНК вируса становится частью нас, и тогда клетки, призванные защищать нас, начинают воспроизводить ДНК вируса.
Вторая проблема весьма уникальна: например, СПИД наконец проявился, люди понимают, что больны и идут в клинику, а у них, мириад других инфекций, что именно стало причиной заболевания. Как это определить? В большинстве случаев вирус существует ради единственной цели: проникнуть в клетку-акцептор и размножиться. Обычно, он прикрепляется к клетке и выпускает в неё свою генетическую информацию. Это позволяет вирусу подчинить себе функции клетки, перенаправив их на производство новых особей вирусов. Затем эти особи нападают на другие клетки. Но ВИЧ — это не рядовой вирус. Он принадлежит к той категории вирусов, которых учёные называют ретровирусами. Что же в них необычного? Подобно тем классам вирусов, куда входят полиомиелит или грипп, ретровирусы — особые категории. Они уникальны тем, что их генетическая информация в виде рибонуклеиновой кислоты конвертируется в дезоксирибонуклеиновую кислоту (ДНК) и как раз то, что происходит с ДНК, и составляет нашу проблему: ДНК встраивается в наши гены, ДНК вируса становится частью нас, и тогда клетки, призванные защищать нас, начинают воспроизводить ДНК вируса. Имеются клетки, содержащие вирус, иногда они воспроизводят его, иногда — нет. Молчат. Затаиваются…Но лишь для того, чтобы потом снова воспроизводить вирус. Т.е. когда инфекция становится очевидной, она, скорее всего, укоренилась на всю жизнь. В этом заключается главная проблема. Лекарство от СПИДа до сих пор не найдено. Но открытие, что ВИЧ — ретровирус, и что он является возбудителем СПИДа, привело к значительным достижениям в борьбе с этим недугом. Что изменилось в медицине после открытия ретровирусов, в особенности ВИЧ? Например, из СПИДа мы убедились, что медикаментозная терапия возможна. Раньше считалось, что поскольку для размножения вирус узурпирует наши клетки, воздействовать на него без тяжёлого отравления самого пациента практически невозможно. Никто не инвестировал антивирусных программ. СПИД открыл дверь антивирусным исследованиям в фармацевтических кампаниях и университетах всего мира. К тому же, СПИД дал положительный социальный эффект. По иронии судьбы, этот ужасный недуг сплачивает людей.
Имеются клетки, содержащие вирус, иногда они воспроизводят его, иногда — нет. Молчат. Затаиваются…Но лишь для того, чтобы потом снова воспроизводить вирус. Т.е. когда инфекция становится очевидной, она, скорее всего, укоренилась на всю жизнь. В этом заключается главная проблема. Лекарство от СПИДа до сих пор не найдено. Но открытие, что ВИЧ — ретровирус, и что он является возбудителем СПИДа, привело к значительным достижениям в борьбе с этим недугом. Что изменилось в медицине после открытия ретровирусов, в особенности ВИЧ? Например, из СПИДа мы убедились, что медикаментозная терапия возможна. Раньше считалось, что поскольку для размножения вирус узурпирует наши клетки, воздействовать на него без тяжёлого отравления самого пациента практически невозможно. Никто не инвестировал антивирусных программ. СПИД открыл дверь антивирусным исследованиям в фармацевтических кампаниях и университетах всего мира. К тому же, СПИД дал положительный социальный эффект. По иронии судьбы, этот ужасный недуг сплачивает людей.
И так день за днем, столетие за столетием, крохотными шажками или грандиозными прорывами, совершались великие и малые открытия в медицине. Они дают надежду, что человечество победит рак и СПИД, аутоиммунные и генетические заболевания, достигнет совершенства в профилактике, диагностике и лечении, облегчая страдания больных людей и предотвращая прогрессирование заболеваний.
Десять великих открытий медицины, изменивших мир
Медицина прошла длинный путь развития для того, чтобы стать такой, какой мы ее сегодня знаем. Сложно представить, что еще каких-то 100-200 лет назад аппендицит мог привести к скоропалительному летальному исходу, а роды нередко заканчивались заражением крови.
В этой статье мы расскажем, какие открытия в медицине были самыми важными и грандиозными.
1. Открытие анестезии
Вплоть до второй половины 19 века всевозможные хирургические операции, в том числе и ампутация конечностей, проводились «на живую». В древности из подобных мероприятий даже делали шоу: посмотреть на банальное вырывание зуба собиралась толпа зевак. Разумеется, не редки случаи, когда вмешательство приводило к болевому шоку. Конец этому беспределу положил американский врач Уильям Мортон, который в 1846 году прилюдно провел процедуру удаления челюстной опухоли спящему пациенту. Публика оценила манипуляцию как чудо. На деле в роли чуда выступил диэтиловый эфир, ставший первым шагом в развитии анестезиологии. Занятно, что Мортон занялся изучением способов обезболивания по причине безденежья: никто не хотел идти к стоматологу удалять зубы из страха.
В древности из подобных мероприятий даже делали шоу: посмотреть на банальное вырывание зуба собиралась толпа зевак. Разумеется, не редки случаи, когда вмешательство приводило к болевому шоку. Конец этому беспределу положил американский врач Уильям Мортон, который в 1846 году прилюдно провел процедуру удаления челюстной опухоли спящему пациенту. Публика оценила манипуляцию как чудо. На деле в роли чуда выступил диэтиловый эфир, ставший первым шагом в развитии анестезиологии. Занятно, что Мортон занялся изучением способов обезболивания по причине безденежья: никто не хотел идти к стоматологу удалять зубы из страха.
2. Антисептика против антисанитарии
Антисанитария – страшный враг Средневековья, ставшая причиной смерти тысяч людей. Плачевная ситуация наблюдалась не только в быту, но и в медицине. Например, хирурги делали операции одними приборами множеству пациентов и даже не мыли руки. В результате, пациенты гибли не от своей патологии, а от заражения крови. Первым, кто попытался изменить ситуацию, стал венгерский хирург Игнац Земмельвейс в 19 веке. Он категорически настаивал на необходимости промывать руки в дезинфицирующем растворе хлорной извести перед взаимодействием с пациентом. Его подход снизил смертность среди рожениц практически в 10 раз. Однако коллеги его идею не оценили и поместили Земмельвейса в психиатрическую клинику, где он и провел остаток своих дней.
Первым, кто попытался изменить ситуацию, стал венгерский хирург Игнац Земмельвейс в 19 веке. Он категорически настаивал на необходимости промывать руки в дезинфицирующем растворе хлорной извести перед взаимодействием с пациентом. Его подход снизил смертность среди рожениц практически в 10 раз. Однако коллеги его идею не оценили и поместили Земмельвейса в психиатрическую клинику, где он и провел остаток своих дней.
Позже английский врач Джозеф Листер реабилитировал репутацию своего коллеги и доказал необходимость стерилизовать хирургические инструменты и обрабатывать рану. Эти открытия спасли миллионы жизней, после чего уже все поверили в их обоснованность.
3. Счастливый случай или открытие антибиотиков
Следующим шагом против бактерий стало изобретение антибиотика. Случилось это в 1928 году. Шотландский медик Александр Флеминг был блестящим ученым, но не любил наводить порядок. Эта черта и помогла ему сделать великое открытие: он забыл о том, что в его лаборатории осталась емкость со стафилококком. Через некоторое время он обнаружил, что в чашке поселились плесневые грибы, которые уничтожили патогенные бактерии. Счастливая случайность, которая в дальнейшем спасет жизни многих людей. За это научное достижение позже он получил Нобелевскую премию, так как открытый им антибиотик активно стал применяться в лечении пневмонии, туберкулёза, малярии и многих других болезней, ранее считавшихся приговором.
Через некоторое время он обнаружил, что в чашке поселились плесневые грибы, которые уничтожили патогенные бактерии. Счастливая случайность, которая в дальнейшем спасет жизни многих людей. За это научное достижение позже он получил Нобелевскую премию, так как открытый им антибиотик активно стал применяться в лечении пневмонии, туберкулёза, малярии и многих других болезней, ранее считавшихся приговором.
4. Рентгеновское излучение
То, что сегодня доступно любой в деревенской больнице, в 19 веке выглядело магией. Зачастую врачи вынуждены были заново ломать неправильно сросшиеся кости пациента в результате перелома. Ведь никто не видел, что происходит внутри, ориентироваться можно было только на ощупь. Занятно, что физик Вильгельм Рентген открыл излучение совершенно случайно. Он проводил опыты в темном кабинете и вдруг обнаружил, что лучи могут проникать через различные предметы, в том числе и через тело человека. Конечно, увидеть человека насквозь на тот момент было шоком. Это открытие дало мощный толчок разным областям медицины, таким как пульмонология, травматология, онкология.
Это открытие дало мощный толчок разным областям медицины, таким как пульмонология, травматология, онкология.
5. Инсулин и сахарный диабет
Сахарный диабет и сегодня занимает одну из лидирующих позиций в мире по числу заболевших и является глобальной проблемой. Полноценная жизнь больных сахарным диабетом без инсулина невозможна. Препарат был открыт только в начале 20 века, когда было установлено, что причина патологии — нехватка гормона поджелудочной железы — инсулина. В 1922 году канадский физиолог Фредерик Бантинг выделили инсулин из поджелудочной железы животных, после чего препарат стали использовать против сахарного диабета у людей. Ученый получил Нобелевскую премию за это изобретение, при том, что на тот момент ему было всего 32 года. Это открытие является поистине мощным прорывом в эндокринологии, ведь до сих пор более эффективного средства борьбы с сахарным диабетом не придумано.
6. Химиотерапия в борьбе с онкологией
Онкологические заболевания до сих относятся к числу загадок, так как никто не может однозначно установить причину их возникновения и спрогнозировать исход лечения. Но, во всяком случае, химиотерапия в части случаев оказывается эффективна, тогда как ранее заболевание не поддавалось никакому лечению. Все началось с того, что польский медик Сидни Фарбер попробовал применить химиотерапию в лечении острой лейкемией у детей. После формирования положительной статистики, препарат был запатентован. По сути, препараты химиотерапии являются ядами, которые ранее использовались как химическое оружие. Их способность уничтожать злокачественные клетки была обнаружена совершенно случайно.
Но, во всяком случае, химиотерапия в части случаев оказывается эффективна, тогда как ранее заболевание не поддавалось никакому лечению. Все началось с того, что польский медик Сидни Фарбер попробовал применить химиотерапию в лечении острой лейкемией у детей. После формирования положительной статистики, препарат был запатентован. По сути, препараты химиотерапии являются ядами, которые ранее использовались как химическое оружие. Их способность уничтожать злокачественные клетки была обнаружена совершенно случайно.
7. Вакцина или прививка против оспы
Чума, тиф и оспа – характерные эпидемии Средневековья, уносящие жизни целых городов и деревень. При чем, критическая ситуация сохранялась вплоть до 19 века. Интересно, что в Китае еще в 10 веке придумали хитрый способ заражать человека небольшой порцией инфекции с целью избежание заражения в будущем. Но, способ давал сбои: нередко такая вакцинация приводила к смерти. Адекватное применение методики было разработано только в конце 19 века. Деревенский доктор Эдвард Дженнер обратил внимание на то, что доярки, заразившиеся оспой от животных, потом успешно избегают человеческой оспы в период эпидемий. Тогда он и решил, что прививки — это шанс спастись от эпидемий. Идея очень не понравилась церкви, а тогда ее влияние на умы было еще слишком высоким. Однако, люди начали делать прививки тайно: в первый год после изобретения прививки сделали более 100 тысяч человек. Открытие Дженнера послужило почвой для создания прививок от многих болезней. В 20 веке эта технология применялась очень активно. В СССР, в частности, многие прививки ставились каждому в обязательном порядке.
Деревенский доктор Эдвард Дженнер обратил внимание на то, что доярки, заразившиеся оспой от животных, потом успешно избегают человеческой оспы в период эпидемий. Тогда он и решил, что прививки — это шанс спастись от эпидемий. Идея очень не понравилась церкви, а тогда ее влияние на умы было еще слишком высоким. Однако, люди начали делать прививки тайно: в первый год после изобретения прививки сделали более 100 тысяч человек. Открытие Дженнера послужило почвой для создания прививок от многих болезней. В 20 веке эта технология применялась очень активно. В СССР, в частности, многие прививки ставились каждому в обязательном порядке.
8. Группы крови
Переливание крови как способ лечения использовалось с древности. Но, так как характеристики крови не были изучены достаточно глубоко, зачастую манипуляции приводили к неожиданным последствиям, в том числе и к летальному исходу. На границе 19 и 20 века иммунолог Карл Ландштейнер выявил индивидуальные характеристики эритроцитов. В своих трудах он доказал, что группа крови – это личная характеристика каждого человека, передающаяся по наследству и отличающаяся свойствами эритроцитов. За это открытие он был удостоен Нобелевской премии. Благодаря этим данным, в медицине активно стали использовать переливание донорской крови для лечения различных патологий и клинических состояний. Важным аспектом явилось открытие того, что кровь необходимо переливать по особым правилам, исключая возможность смешения конфликтующих видов крови.
В своих трудах он доказал, что группа крови – это личная характеристика каждого человека, передающаяся по наследству и отличающаяся свойствами эритроцитов. За это открытие он был удостоен Нобелевской премии. Благодаря этим данным, в медицине активно стали использовать переливание донорской крови для лечения различных патологий и клинических состояний. Важным аспектом явилось открытие того, что кровь необходимо переливать по особым правилам, исключая возможность смешения конфликтующих видов крови.
9. Витамины. Расцвет медицины 20 века.
Это сегодня каждый заботящийся о здоровье человек следит за поддержанием уровня витаминов в организме. Еще несколько веков назад никто толком и не знал, что это за зверь – витамины. Хотя, например на Руси, знахари многое знали о целебной силе различных трав и растений. Впервые о витаминах заговори в 18 веке, когда шотландский врач Джеймс Линд предложил лечить моряков, больных цингой, витамином С. Медицинское сообщество засмеяло его идею. И совершенно зря, ведь сегодня уже доподлинно известно, что цинга возникает от острого дефицита витамина С и других витаминов.
И совершенно зря, ведь сегодня уже доподлинно известно, что цинга возникает от острого дефицита витамина С и других витаминов.
Открыть тайную природу витаминов пытались многие ученые. Однако сделать это удалось двум европейским врачам Фредерику Хопкинсу и Христиану Эйкману, которые получили Нобелевскую премию за свои труды о витаминах. В 20 веке эти знания стали активно распространяться и применяться в медицине.
10. Генетические тесты – основа медицины нового поколения
Поистине грандиозное открытие нашего времени. Сегодня ДНК-тестирования используются в медицине для выявления генетических особенностей организма и предрасположенностей к различным заболеваниям и патологиям. Генетика, как наука, прошла огромный путь развития от древности и до наших дней: великие открытия в этой области можно перечислять очень долго. В 1984 году генетиком Алеком Джеффризом было установлено, что ДНК каждого человека является уникальным и не меняется в течение всей жизни. К концу века уже был полностью расшифрован геном человека.
К концу века уже был полностью расшифрован геном человека.
Первоначально, генетические тестирования начали активно использовать в криминалистике для раскрытия преступлений. Так, в 1987 году в Великобритании ДНК-анализ впервые был применен для доказательства виновности в убийстве. Через год, в 1988 году, ДНК-тесты стали применять и криминалисты в СССР. Впервые использовать ДНК-тесты для медицинских целей стала американская компания Myriad Genetics в начале 2000-х, которая делала тесты для выявления предрасположенности к раку. Сегодня рынок генетических тестирований распространяется по всему цивилизованному миру. ДНК-тесты используют для составления генеалогического древа, для установления отцовства и иных родственных связей, для выявления особенностей метаболизма и усвоения пищи в диетологии, для анализа характеристик кожи в косметологии, для изучения генетических особенностей гормональной системы и подбора адекватной гормональной терапии в эндокринологии и во многих других сферах медицины для анализа предрасположенностей к различным заболеваниям. Это дает реальную возможность заранее спрогнозировать риск патологии и избежать или минимизировать его при помощи профилактики и своевременного лечения.
Это дает реальную возможность заранее спрогнозировать риск патологии и избежать или минимизировать его при помощи профилактики и своевременного лечения.
Ученые оценили значение открытия нобелевских лауреатов по медицине — РБК
Во время пресс-конференции в Каролинском институте после объявления лауреатов Нобелевской премии по физиологии и медицине (Фото: Jessica Gow / EPA / ТАСС)
Открытие рецепторов температуры и прикосновения, которое сделали лауреаты Нобелевской премии по физиологии и медицине этого года Ардем Патапутян и Дэвид Джулиус, поможет изучить так называемые сезонные заболевания. Об этом рассказал РБК кандидат биологических наук, доцент Санкт-Петербургского государственного университета, физиолог Ринад Минвалеев.
Об этом рассказал РБК кандидат биологических наук, доцент Санкт-Петербургского государственного университета, физиолог Ринад Минвалеев.
«Понимание молекулярных механизмов воздействия позволит понять, как использовать их для прямого влияния. Изучить ряд феноменов — например, почему от холода мы испытываем так называемую холодовую усталость, которая может привести к снижению иммунитета. Лучше изучить заболевания, которые мы называем сезонными за связь с определенным временем года», — сказал он.
Нобелевку по медицине присудили за открытие рецепторов температурыПо его словам, хотя о наличии тепловых рецепторов было известно давно, Нобелевскую премию вручили за полное выявление механизма их действия — того, как эти сигналы молекулярно преобразуются организмом в другие, а после — воспринимаются центральной нервной системой.
«Премию вручили за исследование того, как эти сигналы молекулярно преобразуются в другие сигналы, которые воспринимаются нашей ЦНС. Объяснение того, как мы воспринимаем тепло, холод, давление», — пояснил ученый.
Нобелевку по медицине присудили за открытие рецепторов температуры — РБК
Обнаруженные нобелиатами «ионные каналы» регулируют важнейшие физиологические процессы, в том числе артериальное давление и дыхание, а результаты исследований используют для разработки методов лечения широкого спектра заболеваний
Фото: Jessica Gow / EPA / ТАСС
Лауреатами Нобелевской премии по физиологии и медицине 2021 года стали американцы Дэвид Джулиус и Ардем Патапутян «за открытие рецепторов температуры и прикосновения».
«Способность ощущать тепло, холод и прикосновения необходима нам для выживания и лежит в основе нашего взаимодействия с окружающим миром. Мы воспринимаем такие ощущения как должное. Как возникают нервные импульсы, которые позволяют нам чувствовать температуру и давление? Ответ на этот вопрос дали лауреаты Нобелевской премии этого года… Их революционные открытия позволили нам понять, как тепло, холод и механическая сила могут инициировать нервные импульсы, которые позволяют нам воспринимать окружающий мир и адаптироваться к нему», — говорится в заявлении Нобелевского комитета.
В сообщении подчеркивается, что обнаруженные нобелиатами «ионные каналы» регулируют важнейшие физиологические процессы, в том числе артериальное давление и дыхание, а результаты исследований используются для разработки методов лечения широкого спектра заболеваний.
Эксперт МИФИ пояснила значение открытия Нобелевских лауреатов по медицине
https://ria. ru/20211005/mifi-1753053450.html
ru/20211005/mifi-1753053450.html
Эксперт МИФИ пояснила значение открытия Нобелевских лауреатов по медицине
Эксперт МИФИ пояснила значение открытия Нобелевских лауреатов по медицине — РИА Новости, 05.10.2021
Эксперт МИФИ пояснила значение открытия Нобелевских лауреатов по медицине
Открытие Джулиуса и Патапутяна, отмеченное нобелевской премией по медицине 2021 года, может лечь в основу перспективных разработок в области реабилитационной… РИА Новости, 05.10.2021
2021-10-05T03:00
2021-10-05T03:00
2021-10-05T03:00
наука
общество
национальный исследовательский ядерный университет «мифи»
здоровье
нобелевская премия
навигатор абитуриента
университетская наука
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://cdnn21.img.ria.ru/images/07e5/0a/04/1753052251_0:69:3086:1805_1920x0_80_0_0_c952e98b386e3407ccc1236dc8492e72.jpg
МОСКВА, 5 окт — РИА Новости. Открытие Джулиуса и Патапутяна, отмеченное нобелевской премией по медицине 2021 года, может лечь в основу перспективных разработок в области реабилитационной медицины, восстановительной терапии и нейробионических протезов, считает доцент Инженерно-физического института биомедицины Национального исследовательского ядерного университета «МИФИ» (ИФИБ НИЯУ МИФИ) Дарима Максарова.Нобелевский комитет присудил премию по медицине за 2021 год ученым Дэвиду Джулиусу и Ардему Патапутяну, изучившим, как живые организмы чувствуют температуру. Исследователи в свое время открыли молекулы-рецепторы, которые запускают биохимические реакции, приводящие к ощущениям тепла, холода или касаний.Открытие Джулиуса и Патапутяна очень важно, как для развития современной медицинской науки, так и для восстановительного лечения пациентов, отметила Дарима Максарова.»Данные по идентификации дополнительных связанных ионных каналов, полученные нобелевскими лауреатами, позволили ученым понять, как разные температуры вызывают электрические сигналы в нервной системе.
Открытие Джулиуса и Патапутяна, отмеченное нобелевской премией по медицине 2021 года, может лечь в основу перспективных разработок в области реабилитационной медицины, восстановительной терапии и нейробионических протезов, считает доцент Инженерно-физического института биомедицины Национального исследовательского ядерного университета «МИФИ» (ИФИБ НИЯУ МИФИ) Дарима Максарова.Нобелевский комитет присудил премию по медицине за 2021 год ученым Дэвиду Джулиусу и Ардему Патапутяну, изучившим, как живые организмы чувствуют температуру. Исследователи в свое время открыли молекулы-рецепторы, которые запускают биохимические реакции, приводящие к ощущениям тепла, холода или касаний.Открытие Джулиуса и Патапутяна очень важно, как для развития современной медицинской науки, так и для восстановительного лечения пациентов, отметила Дарима Максарова.»Данные по идентификации дополнительных связанных ионных каналов, полученные нобелевскими лауреатами, позволили ученым понять, как разные температуры вызывают электрические сигналы в нервной системе. Эти данные могут иметь практическое применение в области реабилитационной медицины, восстановительной терапии при постинсультных состояниях, в гериатрии (при профилактике и лечении возрастных заболеваний)», — рассказала она.По ее мнению, результаты исследования могут иметь важное применение при разработке мероприятий в области адаптационной медицины (поддержании гомеостаза организма в экстремальных и субэкстремальных условиях, например, при работе в Арктике, Антарктике или в космосе), а также при разработке новых лекарств – анестетиков и спазмолитических препаратов.»Сегодня как никогда быстро развиваются реабилитационные технологии, расширяется сфера применения нейроинтерфейсов, которые базируются на открытиях нейрофизиологии, молекулярной биологии и достижениях в области цифровых технологий. В частности, можно ожидать, что открытие нобелевских лауреатов даст импульс усовершенствованию нейробионических протезов конечностей и откроет новые горизонты в области ассистивных технологий», — заключила Максарова.
Эти данные могут иметь практическое применение в области реабилитационной медицины, восстановительной терапии при постинсультных состояниях, в гериатрии (при профилактике и лечении возрастных заболеваний)», — рассказала она.По ее мнению, результаты исследования могут иметь важное применение при разработке мероприятий в области адаптационной медицины (поддержании гомеостаза организма в экстремальных и субэкстремальных условиях, например, при работе в Арктике, Антарктике или в космосе), а также при разработке новых лекарств – анестетиков и спазмолитических препаратов.»Сегодня как никогда быстро развиваются реабилитационные технологии, расширяется сфера применения нейроинтерфейсов, которые базируются на открытиях нейрофизиологии, молекулярной биологии и достижениях в области цифровых технологий. В частности, можно ожидать, что открытие нобелевских лауреатов даст импульс усовершенствованию нейробионических протезов конечностей и откроет новые горизонты в области ассистивных технологий», — заключила Максарова.
https://ria.ru/20211004/premiya-1752971272.html
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
2021
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
Новости
ru-RU
https://ria.ru/docs/about/copyright.html
https://xn--c1acbl2abdlkab1og.xn--p1ai/
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
https://cdnn21.img.ria.ru/images/07e5/0a/04/1753052251_355:0:3086:2048_1920x0_80_0_0_3fed8510483b317c9e9b044ba45e032b.jpgРИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
РИА Новости
internet-group@rian. ru
ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
общество, национальный исследовательский ядерный университет «мифи», здоровье, нобелевская премия, навигатор абитуриента, университетская наука
МОСКВА, 5 окт — РИА Новости. Открытие Джулиуса и Патапутяна, отмеченное нобелевской премией по медицине 2021 года, может лечь в основу перспективных разработок в области реабилитационной медицины, восстановительной терапии и нейробионических протезов, считает доцент Инженерно-физического института биомедицины Национального исследовательского ядерного университета «МИФИ» (ИФИБ НИЯУ МИФИ) Дарима Максарова.Нобелевский комитет присудил премию по медицине за 2021 год ученым Дэвиду Джулиусу и Ардему Патапутяну, изучившим, как живые организмы чувствуют температуру. Исследователи в свое время открыли молекулы-рецепторы, которые запускают биохимические реакции, приводящие к ощущениям тепла, холода или касаний.
Открытие Джулиуса и Патапутяна очень важно, как для развития современной медицинской науки, так и для восстановительного лечения пациентов, отметила Дарима Максарова.
«Данные по идентификации дополнительных связанных ионных каналов, полученные нобелевскими лауреатами, позволили ученым понять, как разные температуры вызывают электрические сигналы в нервной системе. Эти данные могут иметь практическое применение в области реабилитационной медицины, восстановительной терапии при постинсультных состояниях, в гериатрии (при профилактике и лечении возрастных заболеваний)», — рассказала она.
По ее мнению, результаты исследования могут иметь важное применение при разработке мероприятий в области адаптационной медицины (поддержании гомеостаза организма в экстремальных и субэкстремальных условиях, например, при работе в Арктике, Антарктике или в космосе), а также при разработке новых лекарств – анестетиков и спазмолитических препаратов.
«Сегодня как никогда быстро развиваются реабилитационные технологии, расширяется сфера применения нейроинтерфейсов, которые базируются на открытиях нейрофизиологии, молекулярной биологии и достижениях в области цифровых технологий. В частности, можно ожидать, что открытие нобелевских лауреатов даст импульс усовершенствованию нейробионических протезов конечностей и откроет новые горизонты в области ассистивных технологий», — заключила Максарова.
Открытия нобелевских лауреатов помогут лечить хронические боли
В этом году Нобелевскую премию по физиологии и медицине (10 млн шведских крон, или $1,15 млн) поровну разделят Дэвид Джулиус из Калифорнийского университета в Сан-Франциско и Ардем Патапутян из Института Скриппса. Присуждение премии за открытия, не имеющие отношения к главной теме, которая сегодня волнует человечество, многих удивило. Газета Daily Mail, например, так и написала в заголовке для интернет-версии: «Нобелевская премия по медицине НЕ досталась исследователям коронавируса», выделив «не» заглавными.
В прошлом году премию получили вирусологи, но не за борьбу с COVID-19, а за открытие вируса гепатита С. Дело в том, что список претендентов на Нобелевку составляется в январе, а в январе 2020 г. эпидемия в Китае казалась локальной проблемой. В январе этого года пандемия уже бушевала по всему миру. Но, как нетрудно заметить, такова нобелевская традиция – отмечать премиями по медицине, физике, химии за открытия, сделанные много лет назад. Нобелевский комитет остался верен себе.
Одно из главных достижений Джулиуса – открытие гена TRPV1, делающего клетку восприимчивой к капсаицину. Это алкалоид, который содержится в различных видах стручкового перца.
Дэвид Джулиус /Noah Berger / UCSF / AFP
Ученые и раньше знали, что капсаицин активирует нервные клетки (кстати, это чувствовал и любой из нас, кому приходилось откусить от стручка чили). Но не известно было, как именно капсаицин это делает. Джулиус и его команда в 1990-х выясняли, каким образом и почему приходят в действие нейроны, а заодно выяснили, что ген TRPV1 отвечает также за реакцию на тепло. Он активируется при температуре выше 43 оС. Так что, когда говорят, что перец жжет, – это правда. Он действительно жжет, организм на него реагирует с помощью тех же механизмов, что и на горячее.
Он активируется при температуре выше 43 оС. Так что, когда говорят, что перец жжет, – это правда. Он действительно жжет, организм на него реагирует с помощью тех же механизмов, что и на горячее.
Затем Джулиус и работавший независимо от него Патапутян обнаружили, что ментол действительно холодит: ген TRPM8 формирует реакцию и на это вещество, и на холод. Дальше Джулиус перебирал разные вещества и изучал реакцию на них, Патапутян разбирался, что заставляет нас ощутить давление. Исследователи давили микропипеткой и воздействовали на клетку в теле мыши, клетка передавала сигнал об этом в мозг, ученые наблюдали за процессом и попутно искусственно отключали один за другим 72 гена до тех пор, пока не нашли искомый. После дезактивации одного из генов клетки перестали реагировать на нажатие. Так было обнаружено, что ген Piezo1 отвечает за ощущение давления. Затем ученые смогли понять, как именно механическое усилие приводит к появлению нервного импульса.
Что в человеческом теле есть некие нити, протянутые от кожи к мозгу, и они реагируют на прикосновение, предположил еще философ Рене Декарт в XVII в. Очень многое человечество выяснило о нервной системе и принципах ее работы в XX в. «Однако до открытий Джулиуса и Патапутяна было не ясно, как именно в нервной системе температурные и механические стимулы преобразуются в электрические импульсы», – объясняется в сообщении Нобелевского комитета.
Очень многое человечество выяснило о нервной системе и принципах ее работы в XX в. «Однако до открытий Джулиуса и Патапутяна было не ясно, как именно в нервной системе температурные и механические стимулы преобразуются в электрические импульсы», – объясняется в сообщении Нобелевского комитета.
Почему эти открытия важны
Как минимум одно из возможных последствий открытия Джулиуса и Патапутяна – избавление от хронических болей. Найденный Джулиусом ген TRPV1 отвечает за определенный ионный канал – это сложные белки, которые, образно говоря, выполняют роль калитки в клеточных мембранах. Ионный канал, играющий роль рецептора, обеспечивает прохождение только определенных катионов или анионов, отобранных из числа многих. То есть через них в клетку и из нее проникают ионы – или же не проникают, если калитка закрыта. От того, сколько положительно и отрицательно заряженных ионов накопилось внутри мембраны и снаружи нее, зависит ее электрический потенциал. Посредством изменения электрического потенциала сигналы, информация передаются от клеток мозгу. Например, когда клетка соприкасается с капсаицином или попадает в пламя, калитка, которую контролирует ген TRPV1, открывается и в мозг поступает информация: это горячо. А обнаруженный Патапутяном ген Piezo1 отвечает за работу своего ионного канала.
Например, когда клетка соприкасается с капсаицином или попадает в пламя, калитка, которую контролирует ген TRPV1, открывается и в мозг поступает информация: это горячо. А обнаруженный Патапутяном ген Piezo1 отвечает за работу своего ионного канала.
«Нашей задачей было разобраться в возникновении боли на молекулярном уровне», – говорил Джулиус в интервью сайту премии Frontiers of Knowledge Award, которую получил тоже вместе с Патапутяном.
«Piezo1 действует при отдельных видах боли, – продолжал объяснения коллеги Патапутян. – Боль от удара молотком не имеет никакой связи с [действием] Piezo1. Но если вы получили солнечный ожог или просто больно касаться плеча, этот вид боли с ним связан. Это может оказаться важно для лечения тех болей [которые ощущаются долгое время после травмы]. Интересно посмотреть за реакцией фармацевтики в следующие 5–10 лет на эти открытия».
Джулиус добавлял в интервью сайту Pain Research Forum: «Проблема в том, что фармацевтическим компаниям трудно работать с болью. Они взялись за нее, а потом отказались [от разработки анальгетиков] в пользу таких вещей, как средства против нейродегенеративных заболеваний и рака Но недавние испытания показали, что работа с TRPV1 может помочь в лечении болей в коленях при остеоартрите и т. д.». Он тоже ждет появления новых лекарств, избавляющих от страданий.
Они взялись за нее, а потом отказались [от разработки анальгетиков] в пользу таких вещей, как средства против нейродегенеративных заболеваний и рака Но недавние испытания показали, что работа с TRPV1 может помочь в лечении болей в коленях при остеоартрите и т. д.». Он тоже ждет появления новых лекарств, избавляющих от страданий.
Мальчик с Брайтон-Бич
Оба ученых работают сейчас в одном штате. Джулиус – профессор и заведующий кафедрой физиологии Калифорнийского университета в Сан-Франциско. Патапутян – профессор и исследователь в отделе неврологии Института Скриппса в Сан-Диего (Калифорния). «Я прожил в Северной Калифорнии более половины жизни, но по темпераменту и юмору остаюсь коренным жителем Нью-Йорка. Я вырос в приморской части Бруклина, увековеченной в пьесе Нила Саймона «Брайтон-Бич, мемуары», – он стал домом для иммигрантов из Восточной Европы, таких как мои бабушка и дедушка, бежавшие из царской России от антисемитизма в поисках лучшей жизни», – рассказывал Джулиус в автобиографии, написанной в прошлом году для сайта премии Кавли (ее он опять-таки получил на пару с Патапутяном и за те же исследования, что и Нобелевку). Джулиус родился в 1955 г. Отец проектировал и обслуживал системы аварийного электроснабжения для телефонной компании, а мать преподавала в школе. Вместе с родителями и двумя братьями они жили этажом ниже бабушки по материнской линии, тети, дяди и двух двоюродных братьев. Бабушка и дедушка по отцовской линии обитали неподалеку в соседних кварталах.
Джулиус родился в 1955 г. Отец проектировал и обслуживал системы аварийного электроснабжения для телефонной компании, а мать преподавала в школе. Вместе с родителями и двумя братьями они жили этажом ниже бабушки по материнской линии, тети, дяди и двух двоюродных братьев. Бабушка и дедушка по отцовской линии обитали неподалеку в соседних кварталах.
И братья, и кузены выбрали карьеру в области инженерного дела, науки, образования и юриспруденции. Так что от Джулиуса тоже ожидали интереса к наукам. Его отдали в бруклинскую государственную школу им. Авраама Линкольна. У нее внушительный список известных выпускников – от знаменитых писателей (Артур Миллер, Джозеф Хеллер, Мел Брукс) до знаменитых ученых: биохимики Артур Корнберг и Пол Берг и химик Джером Карле тоже нобелевские лауреаты (1959, 1980 и 1985 г. соответственно). При Джулиусе ученический состав был не столь легендарным, но он нашел много интересных и умных приятелей. Они ходили по концертам, музеям и даже бродвейским шоу, благо, как шутит Джулиус, в те времена динамическое ценообразование еще не было так развито. А летом вся компания играла в баскетбол или резвилась на пляже в окружении миллиона других ньюйоркцев, выбравшихся из небоскребов к воде.
А летом вся компания играла в баскетбол или резвилась на пляже в окружении миллиона других ньюйоркцев, выбравшихся из небоскребов к воде.
Джулиусу повезло дважды. Во-первых, когда бейсболист низшей лиги Херб Исааксон некогда отказался от мечты стать спортсменом и подался в учителя. Во-вторых, когда Исааксон преподавал физику в классе Джулиуса. Исааксон не перечислял на уроках факты, он бросал в класс идеи для обсуждения и ожидал в ответ жаркие споры. Он сделал физику забавной, увлекательной и имеющей непосредственное отношение к любимому американцами бейсболу, вспоминал Джулиус.
Вот так он увлекся наукой. Вслед за старшим братом Джулиус вознамерился поступить в Университет Нью-Йорка. Но приятель-одноклассник посоветовал подать документы в Массачусетский технологический институт (MIT). Джулиус о таком впервые слышал. Никто из его родственников не учился в частном университете, так что попытаться было интересно. Джулиус вспоминал, что последовал совету, не особенно веря в успех, и очень удивился, когда обнаружил в почтовом ящике письмо о зачислении в MIT.
Научные странствия
В MIT Джулиус был в восторге от программы, позволяющей студентам не тупо повторять известные опыты, а помогать ученым в исследованиях по новым темам. И даже лабораторию можно было выбрать самостоятельно. Джулиус заинтересовался исследованиями ДНК и РНК, и порой у него было ощущение, что он не учится, а удовлетворяет собственное любопытство за чужой счет. Особенно когда он встретил коллег, прибывших поработать в MIT из Франции, и договорился с ними о стажировке в Старом Свете. В перерывах между изучением РНК, извлеченной из зародышей пшеницы и дрожжей, Джулиус наслаждался красотами Бордо и учился разбираться в красном вине.
В Бордо он окончательно решил сделать карьеру в области биомедицинских исследований. Но он получал отказы на свои заявки на работу, пока в самом конце учебного года не подвернулось место в аспирантуре Калифорнийского университета в Беркли. Там Джулиус увлекся новой темой: фармакологией галлюциногенов, опиатов и т. п. Он вдохновлялся трудами популяризатора этой темы Тимоти Лири, книгами Тома Вулфа, писавшего о контркультуре 1960-х, работами ученых – например, Джорджа Агаджаняна, профессора Йельской школы медицины, изучавшего действие ЛСД.
Известно, что содержащиеся в галлюциногенах моноамины взаимодействуют с разными участками мозга. Но было не понятно, как этот процесс выглядит на молекулярном уровне. Джулиус наткнулся на статью об исследовании, которое имело отношение к решению этой загадки. Нейробиолог и биохимик Ричард Шеллер с коллегами изучал, как комплементарная ДНК влияет на поведение морских улиток Aplysia. Джулиус связался с ученым и на шесть с лишним лет вернулся в родной Нью-Йорк, чтобы работать в лаборатории Шеллера в Колумбийском университете.
Набравшись опыта, Джулиус отправился в самостоятельное плавание. В конце 1989 г. он устроился преподавателем в Калифорнийском университете в Сан-Франциско и получил собственную лабораторию. Однако в области, которой он посвятил предыдущие годы, работало слишком много ученых. Джулиус, как он писал в автобиографии, решил заняться сферой, где было мало конкуренции и больше шансов совершить открытие. Поэтому и переключился на исследование ионных каналов. На идею использовать для этого капсаицин его натолкнули труды Николаса Янсо и его коллег из Венгрии в 1940-х гг. – тогда ученые установили, что это вещество является селективным активатором группы нейронов соматосенсорной системы. «Идентифицировать мифический рецептор капсаицина – для меня это стало чем-то вроде Святого Грааля», – вспоминал Джулиус.
На идею использовать для этого капсаицин его натолкнули труды Николаса Янсо и его коллег из Венгрии в 1940-х гг. – тогда ученые установили, что это вещество является селективным активатором группы нейронов соматосенсорной системы. «Идентифицировать мифический рецептор капсаицина – для меня это стало чем-то вроде Святого Грааля», – вспоминал Джулиус.
От конкуренции к дружбе
Патапутян родился в 1967 г. в Ливане в семье выходцев из Армении. В 1986 г., когда в стране шла гражданская война, а потом еще начался конфликт в Южном Ливане, семья эмигрировала в США. Там Патапутян получил степень бакалавра в Калифорнийском университете в Лос-Анджелесе, затем стал доктором биологии в Калифорнийском технологическом институте. Уезжая в Америку, Патапутян думал стать врачом. Но студентом он буквально влюбился в исследовательскую работу.
Ардем Патапутян /Reuters
Так что вместо клиники Патапутян в 1996 г. отправился в лабораторию Калифорнийского университета в Сан-Франциско. К тому времени там уже несколько лет работал над своими исследованиями Джулиус. В 1997 г. Джулиус с коллегами опубликовали статью об открытии гена рецептора капсаицина. Тема заинтересовала и Патапутяна. Независимо от Джулиуса он тоже стал изучать молекулярные основы сенсорного восприятия и начал эксперименты с ментолом в то же время, что и Джулиус.
К тому времени там уже несколько лет работал над своими исследованиями Джулиус. В 1997 г. Джулиус с коллегами опубликовали статью об открытии гена рецептора капсаицина. Тема заинтересовала и Патапутяна. Независимо от Джулиуса он тоже стал изучать молекулярные основы сенсорного восприятия и начал эксперименты с ментолом в то же время, что и Джулиус.
На сайте премии Frontiers of Knowledge Award и Джулиус, и Патапутян признавались, что поначалу были жесточайшими конкурентами. Но потом их работа стала, по словам обоих, «взаимодополняющей». Дело в том, что Патапутян переключился на исследование других рецепторов, нежели Джулиус, и в 2000 г. перешел в Институт Скриппса в Калифорнии. Там он занимает должность профессора неврологии, совмещая ее с работой исследователя в Медицинском институте Говарда Хьюза.
Внимание Патапутяна привлекли исследования американца Альберта Джеймса Хадспета, с 1970-х гг. изучавшего механобиологию слуха. Тот пытался понять, каким образом механическое воздействие звуковых волн на волосковые клетки порождает нервный импульс. Выяснить это удалось Патапутяну. Он разобрался, как благодаря ионным каналам мы способны чувствовать давление. «До сих пор мы относились к [живому организму] как к мешку химических веществ, где информация передается путем химического синтеза, – объяснял Патапутян на сайте Frontiers of Knowledge Award. – Но все больше и больше мы понимаем, что механобиология, механические силы играют важную роль во всем, от деления клеток до слуха, осязания и боли. То, что мы открыли, очень захватывающе, но это лишь верхушка айсберга этой новой науки».
Выяснить это удалось Патапутяну. Он разобрался, как благодаря ионным каналам мы способны чувствовать давление. «До сих пор мы относились к [живому организму] как к мешку химических веществ, где информация передается путем химического синтеза, – объяснял Патапутян на сайте Frontiers of Knowledge Award. – Но все больше и больше мы понимаем, что механобиология, механические силы играют важную роль во всем, от деления клеток до слуха, осязания и боли. То, что мы открыли, очень захватывающе, но это лишь верхушка айсберга этой новой науки».
Уже второй год из-за пандемии нобелевская церемония происходит онлайн. А потом медаль вручают в посольстве Швеции или ее передает из рук в руки один из прежних лауреатов.
Секретарь Нобелевского комитета Томас Перлманн не смог дозвониться Патапутяну, чтобы сообщить о награждении. У лауреата телефон стоял в режиме «не беспокоить», пропуская только вызовы из ограниченного списка номеров. Каким-то образом Перлманн нашел телефон 92-летнего отца Патапутяна, который дозвонился до сына с радостным известием. В твиттере Нобелевского комитета есть фотография, как Патапутян и его сын, лежа в кровати, наблюдают за церемонией оглашения имен победителей. Ученый на фото по-домашнему небрит, но еще недавно его лицо украшали пышные усы. 14 августа этого года Патапутян опубликовал в своем твиттере опрос: что делать с усами? Так как он не звезда TikTok и не исполнитель попсы, а всего лишь ученый, голосующих набралось немного. Свое мнение высказало 160 человек, приговор был – «сбрить». Сейчас, после вручения премии, интерес к этому опросу был бы явно больше.
В твиттере Нобелевского комитета есть фотография, как Патапутян и его сын, лежа в кровати, наблюдают за церемонией оглашения имен победителей. Ученый на фото по-домашнему небрит, но еще недавно его лицо украшали пышные усы. 14 августа этого года Патапутян опубликовал в своем твиттере опрос: что делать с усами? Так как он не звезда TikTok и не исполнитель попсы, а всего лишь ученый, голосующих набралось немного. Свое мнение высказало 160 человек, приговор был – «сбрить». Сейчас, после вручения премии, интерес к этому опросу был бы явно больше.
Есть в твиттере и фото Джулиуса, который дома, в халате, получает известие о своем награждении. Затем опубликовано фото, как они с женой отмечают эту новость кружкой кофе. Супруга Джулиуса работает, как и он, в Калифорнийском университете в Сан-Франциско. Она известна своими исследованиями в области нейроэндокринной физиологии. Вместе они вырастили сына, чьи интересы лежат в сфере искусства. Хотя Джулиус тоже не чужд искусству. «И жена, и сын терпят мои потуги играть на трубе», – признавался он в автобиографии.
Нобелевскую премию по физиологии и медицине вручили за исследование рецепторов температуры и осязания
Автор фото, EPA / Reuters
Нобелевский комитет в Стокгольме назвал имя лауреатов премии в области медицины или физиологии. Ими стали Дэвид Джулиус и Ардем Патапутян. Они открыли, каким образом температура или, например, прикосновение превращаются в человеческие ощущения.
Открытие Джулиуса и Патапутяна нобелевское жюри сочло прорывным. «Лауреаты нынешнего года позволили нам понять, как температура или механическая сила инициируют нервные импульсы, которые позволяют нам воспринимать мир и адаптироваться», — заявили в комитете.
Эта технология потенциально может применяться в разных областях — от медицины до виртуальной реальности и роботостроения.
Премия в области медицины вручается, по словам члена Нобелевской ассамблеи профессора Джулин Зират, «по очень узким критериям».
«Мы искали открытие, которое открыло двери и помогло нам увидеть проблему в новом свете», — говорит она.
«Уровень открытия должен быть очень высоким. Это не может быть изобретением или усовершенствованием чего-то существующего. Должно быть именно открытие», — добавила она в интервью перед вручением премии.
Автор фото, Getty Images
Подпись к фото,Из-за пандемии премию в этом году вручали дистанционно
Родившийся в 1955 году Джулиус работает в Калифорнийском университете в Сан-Франциско и в последние десятилетия изучает молекулярные механизмы, помогающие людям ощущать прикосновение и боль. Группа ученых под его руководством выявила целое семейство чувствительных к температуре рецепторов, позволяющих нервным волокнам определять высокие и низкие температуры, используя свойства натуральных продуктов, в частности, острого перца.
Автор фото, Steve Babuljak
Подпись к фото,Дэвид Джулиус
Ардем Патапутян родился в Бейруте в 1967 году. Он тоже работает в Калифорнии, в медицинском институте Говарда Хьюза.
Он тоже работает в Калифорнии, в медицинском институте Говарда Хьюза.
В его лаборатории удалось выявить и описать ионные каналы, которые активируются изменениями тепловой энергии и, таким образом, функционируют как молекулярные термометры человеческого организма.
Анализ: загадка природы
Николай Воронин, корреспондент Би-би-си по науке
Представьте, что вы решили босиком прогуляться по утреннему полю и идете по прохладной, набухшей росой траве…
Стоп! Откуда вы знаете, что трава прохладная? Что она покрыта росой?
Мы настолько привыкли доверять своим органам чувств, что редко задумываемся о том, как именно они работают. На ощупь отличить холодный предмет от горячего, а твердый от мягкого (ученые называют эту способность соматосенсорикой) не составляет труда даже с закрытыми глазами. Но как мы это делаем — что за механизм лежит в основе этих ощущений — наука не могла объяснить на протяжении тысячелетий. Еще в XVII веке французский философ Рене Декарт предположил, что раз при попадании на кожу огня мы чувствуем ожог и боль, она должна быть каким-то образом связана с мозгом, чтобы передать туда соответствующий сигнал.
Еще в XVII веке французский философ Рене Декарт предположил, что раз при попадании на кожу огня мы чувствуем ожог и боль, она должна быть каким-то образом связана с мозгом, чтобы передать туда соответствующий сигнал.
В конце XIX века на коже были обнаружены чувствительные точки, реагирующие на тот или иной раздражитель, но — опять же — как и почему это происходит, оставалось загадкой.
В 1906 Камилло Гольджи и Сантьяго Рамон-и-Кахаль получили Нобелевскую премию за описание структуры нервной системы. В 1932 награду разделили Чарлз Шеррингтон и Эдгар Эдриан — за «открытия, касающиеся функций нейронов», в том числе соматосенсорных. Еще 12 лет спустя, в 1944, премия была присуждена Джозефу Эрлангеру и Герберту Спенсеру Гассеру — за описание различных функций, которые могут выполнять одиночные нервные волокна.
Дэвид Джулиус заметил, что острая пища вызывает в организме точно такую же реакцию, как и горячая — и предположил, что алкалоид капсаицин (именно обеспечивает жгучий вкус разным видам перца) активирует некий специфический фрагмент ДНК — тот же, что и высокая температура. Перебрав тысячи вариантов, он, наконец, обнаружил ответственный за эту реакцию белок, получивший название TRPV1. А следом и второй — TRPV2, реагирующий на еще более высокую температуру.
Перебрав тысячи вариантов, он, наконец, обнаружил ответственный за эту реакцию белок, получивший название TRPV1. А следом и второй — TRPV2, реагирующий на еще более высокую температуру.
Белок, ответственный за ощущение холода, оба лауреата открыли почти одновременно, в 2002 году. А вот с протеином, обеспечивающим ощущение физического прикосновения, Ардему Патапутяну не повезло. Профессор составил список из 72 генов — потенциальных кандидатов на роль осязательного рецептора — и начал отключать их один за другим, проверяя, не пропало ли осязание. Нужный ген оказался последним, 72-м.
Таким образом ученые выяснили, как именно соматосенсорная система позволяет нам чувствовать не только температуру и прикосновение, но и боль, и даже движение собственного тела. Неудивительно, что в решении Нобелевского комитета сказано, что научные работы новоиспеченных лауреатов «раскрыли одну из загадок природы, на молекулярном уровне объяснив […] нашу способность воспринимать и интерпретировать как окружающий мир, так и наши собственные внутренние ощущения».
На этой неделе нобелевский комитет объявит обладателей премии еще в четырех областях. Во вторник объявят обладателя премии по физике, в среду — по химии, в четверг — по литературе. 11 октября объявят лауреатов премии в области экономики.
В пятницу в столице Норвегии будет объявлен лауреат Нобелевской премии мира. На нее претендуют 329 кандидатов.
10 лучших достижений медицины в истории
На протяжении всей истории болезни вызывали в равной мере страх и восхищение. Однако каждое революционное медицинское открытие приближало нас к пониманию сложных загадок болезней и медицины. В результате мы смогли разработать лекарства и методы лечения, которые помогли спасти миллионы жизней.
Вот хронологический список лучших медицинских достижений в истории на данный момент:
Вакцины (1796)
Трудно точно определить, когда вакцины стали общепринятой практикой, в основном потому, что путь к открытиям был долгим и сложным.
 Начиная с попытки Эдварда Дженнера в 1796 году использовать прививки для приручения печально известного вируса оспы, полезность и популярность вакцин росли очень быстро. На протяжении 1800-х и начале 1900-х годов были созданы различные вакцины для борьбы с некоторыми из самых смертоносных болезней в мире, включая оспу, бешенство, туберкулез и холеру. За 200 лет одна из самых смертоносных болезней, известных человеку — оспа — была стерта с лица земли. С тех пор практически все вакцины работают по одной и той же концепции.Так было до тех пор, пока не появилась новая технология, называемая мРНК, которая создала революционные возможности для будущего здравоохранения. Его высокая эффективность, способность к быстрому развитию и потенциал низких производственных затрат были очевидны во время пандемии Covid-19, две отдельные мРНК-вакцины были разработаны и одобрены для использования всего за несколько месяцев.
Начиная с попытки Эдварда Дженнера в 1796 году использовать прививки для приручения печально известного вируса оспы, полезность и популярность вакцин росли очень быстро. На протяжении 1800-х и начале 1900-х годов были созданы различные вакцины для борьбы с некоторыми из самых смертоносных болезней в мире, включая оспу, бешенство, туберкулез и холеру. За 200 лет одна из самых смертоносных болезней, известных человеку — оспа — была стерта с лица земли. С тех пор практически все вакцины работают по одной и той же концепции.Так было до тех пор, пока не появилась новая технология, называемая мРНК, которая создала революционные возможности для будущего здравоохранения. Его высокая эффективность, способность к быстрому развитию и потенциал низких производственных затрат были очевидны во время пандемии Covid-19, две отдельные мРНК-вакцины были разработаны и одобрены для использования всего за несколько месяцев.
Анестезия (1846)
До первого использования общего анестетика в середине 19 века хирургическое вмешательство применялось только в крайнем случае, когда несколько пациентов предпочитали смерть, а не переносили мучительные испытания. Хотя раньше проводилось бесчисленное количество экспериментов с анестетиком, датируемых 4000 годом до нашей эры, Уильям Т. Г. Мортон вошел в историю в 1846 году, когда он успешно применил эфир в качестве анестетика во время операции. Вскоре после этого стало широко использоваться более быстродействующее вещество под названием хлороформ, но оно считалось высокорисковым после того, как было зарегистрировано несколько смертельных случаев. С 1800-х годов были разработаны более безопасные анестетики, позволяющие проводить миллионы жизненно важных и безболезненных операций.
Хотя раньше проводилось бесчисленное количество экспериментов с анестетиком, датируемых 4000 годом до нашей эры, Уильям Т. Г. Мортон вошел в историю в 1846 году, когда он успешно применил эфир в качестве анестетика во время операции. Вскоре после этого стало широко использоваться более быстродействующее вещество под названием хлороформ, но оно считалось высокорисковым после того, как было зарегистрировано несколько смертельных случаев. С 1800-х годов были разработаны более безопасные анестетики, позволяющие проводить миллионы жизненно важных и безболезненных операций.
Теория зародышей (1861)
До появления теории «микробов» широко распространенной была теория, согласно которой болезнь вызывается «спонтанным зарождением».Другими словами, врачи того времени думали, что болезнь могла возникнуть из воздуха, а не передаваться по воздуху или передаваться через контакт кожа к коже. В 1861 году французский микробиолог Луи Пастер с помощью простого эксперимента доказал, что инфекционное заболевание является результатом вторжения конкретных микроскопических организмов, также известных как патогены, в живых хозяев. Это новое понимание стало важным поворотным моментом в том, как лечить, контролировать и предотвращать болезни, помогая предотвращать разрушительные эпидемии, вызывающие тысячи смертей каждый год, такие как чума, дизентерия и брюшной тиф.
Это новое понимание стало важным поворотным моментом в том, как лечить, контролировать и предотвращать болезни, помогая предотвращать разрушительные эпидемии, вызывающие тысячи смертей каждый год, такие как чума, дизентерия и брюшной тиф.
Медицинская визуализация (1895)
Первыми аппаратами для медицинской визуализации были рентгеновские лучи. Рентгеновское излучение, разновидность электромагнитного излучения, было «случайно» изобретено в 1895 году немецким физиком Вильгельмом Конрадом Рентгеном, когда он экспериментировал с электрическими токами через стеклянные электронно-лучевые трубки. Открытие изменило медицину в одночасье, и к следующему году в больнице Глазго открылось самое первое в мире отделение радиологии.
Ультразвук, впервые открытый много лет назад, начал использоваться для медицинской диагностики в 1955 году. Это медицинское устройство визуализации использует высокочастотные звуковые волны для создания цифрового изображения и было не чем иным, как новаторским с точки зрения обнаружения внутриутробных состояний и других аномалий таза и брюшной полости. В 1967 году был создан сканер компьютерной томографии (КТ), который использует детекторы рентгеновского излучения и компьютеры для диагностики многих различных типов заболеваний и стал основным диагностическим инструментом в современной медицине.
Это медицинское устройство визуализации использует высокочастотные звуковые волны для создания цифрового изображения и было не чем иным, как новаторским с точки зрения обнаружения внутриутробных состояний и других аномалий таза и брюшной полости. В 1967 году был создан сканер компьютерной томографии (КТ), который использует детекторы рентгеновского излучения и компьютеры для диагностики многих различных типов заболеваний и стал основным диагностическим инструментом в современной медицине.
Следующая крупная технология медицинской визуализации была открыта в 1973 году, когда Пол Лаутербур произвел первое магнитно-резонансное изображение (МРТ).Данные ядерного магнитного резонанса создают подробные изображения внутри тела и являются важным инструментом для обнаружения опасных для жизни состояний, включая опухоли, кисты, повреждения головного и спинного мозга, а также некоторые проблемы с сердцем и печенью.
Антибиотики (1928)
Пенициллин Александра Флеминга, первый в мире антибиотик, полностью произвел революцию в войне против смертоносных бактерий. Известно, что шотландский биолог случайно обнаружил антибактериальную «плесень» в чашке Петри в 1928 году.Однако невероятные открытия Флеминга не получили должного признания до 1940-х годов, когда они начали массово производиться американскими фармацевтическими компаниями для использования во время Второй мировой войны. Два других ученых были ответственны за массовое распространение пенициллина, австралиец Говард Флори и беженец из нацистской Германии Эрнст Чейн, и их разработка этого вещества в конечном итоге спасла миллионы будущих жизней. К сожалению, с годами определенные бактерии стали все более устойчивыми к антибиотикам, что привело к всемирному кризису, который требует от фармацевтической промышленности как можно скорее разработать новые антибактериальные препараты.
Известно, что шотландский биолог случайно обнаружил антибактериальную «плесень» в чашке Петри в 1928 году.Однако невероятные открытия Флеминга не получили должного признания до 1940-х годов, когда они начали массово производиться американскими фармацевтическими компаниями для использования во время Второй мировой войны. Два других ученых были ответственны за массовое распространение пенициллина, австралиец Говард Флори и беженец из нацистской Германии Эрнст Чейн, и их разработка этого вещества в конечном итоге спасла миллионы будущих жизней. К сожалению, с годами определенные бактерии стали все более устойчивыми к антибиотикам, что привело к всемирному кризису, который требует от фармацевтической промышленности как можно скорее разработать новые антибактериальные препараты.
Трансплантация органов (1954)
В декабре 1954 года доктор Джозеф Мюррей и доктор Дэвид Хьюм провели первую успешную трансплантацию почки в Бостоне, США. Несмотря на многие предыдущие попытки в истории, это был первый случай, когда реципиент трансплантата органа выжил после операции. Поворотный момент наступил, когда были преодолены различные технические проблемы, такие как сосудистый анастомоз (соединение между двумя кровеносными сосудами), размещение почки и иммунный ответ.В 1963 году была проведена первая трансплантация легких, за ней последовала трансплантация поджелудочной железы / почки в 1966 году и печени и сердца в 1967 году. Помимо спасения тысяч жизней в последующие годы, процедуры трансплантации также становятся все более инновационными и сложными, с участием врачей. успешно завершила первую трансплантацию руки в 1998 году и трансплантацию всего лица в 2010 году!
Поворотный момент наступил, когда были преодолены различные технические проблемы, такие как сосудистый анастомоз (соединение между двумя кровеносными сосудами), размещение почки и иммунный ответ.В 1963 году была проведена первая трансплантация легких, за ней последовала трансплантация поджелудочной железы / почки в 1966 году и печени и сердца в 1967 году. Помимо спасения тысяч жизней в последующие годы, процедуры трансплантации также становятся все более инновационными и сложными, с участием врачей. успешно завершила первую трансплантацию руки в 1998 году и трансплантацию всего лица в 2010 году!
Противовирусные препараты (1960-е годы)
Ужасные вирусы, такие как оспа, грипп и гепатит, на протяжении всей истории уничтожали многие человеческие популяции.В отличие от стремительного успеха антибиотиков в конце 1930-х и 1940-х годах, разработка противовирусных препаратов не началась до 1960-х годов. В основном это было связано со структурой вируса, который представлял собой ядро генетического материала, окруженное защитной белковой оболочкой, которая скрывается и воспроизводится внутри клеток человека. Поскольку информация о вирусах настолько защищена, их было трудно лечить, не повредив клетку-хозяина. За прошедшие годы антивирусные препараты значительно улучшились и работают, блокируя быстрое размножение вирусных инфекций, а некоторые даже могут стимулировать иммунную систему к атаке вируса.Разработка эффективных противовирусных препаратов сыграла важную роль в лечении и сдерживании распространения смертельных вирусных вспышек, таких как ВИЧ / СПИД, Эбола и бешенство.
Поскольку информация о вирусах настолько защищена, их было трудно лечить, не повредив клетку-хозяина. За прошедшие годы антивирусные препараты значительно улучшились и работают, блокируя быстрое размножение вирусных инфекций, а некоторые даже могут стимулировать иммунную систему к атаке вируса.Разработка эффективных противовирусных препаратов сыграла важную роль в лечении и сдерживании распространения смертельных вирусных вспышек, таких как ВИЧ / СПИД, Эбола и бешенство.
Терапия стволовыми клетками (1970-е годы)
Невероятный потенциал стволовых клеток был открыт в конце 1970-х, когда они были обнаружены в пуповинной крови человека. Стволовые клетки примечательны двумя особенностями: это неспециализированные клетки, которые могут обновляться посредством деления клеток даже после того, как они неактивны, и при определенных условиях могут использоваться для создания любых типов клеток человека.Это открытие имеет огромный потенциал, и терапия стволовыми клетками уже используется для лечения лейкемии и других заболеваний крови, а также при трансплантации костного мозга. В настоящее время продолжаются исследования по использованию стволовых клеток для лечения травм спинного мозга и ряда неврологических заболеваний, таких как болезнь Альцгеймера, Паркинсона и инсульты. Однако из-за этических проблем, связанных с использованием эмбриональных стволовых клеток, исследователи, вероятно, столкнутся со многими препятствиями при разработке терапии на основе стволовых клеток.
В настоящее время продолжаются исследования по использованию стволовых клеток для лечения травм спинного мозга и ряда неврологических заболеваний, таких как болезнь Альцгеймера, Паркинсона и инсульты. Однако из-за этических проблем, связанных с использованием эмбриональных стволовых клеток, исследователи, вероятно, столкнутся со многими препятствиями при разработке терапии на основе стволовых клеток.
Иммунотерапия (1970-е годы)
Иммунотерапия, лечение, которое стимулирует иммунную систему для борьбы с болезнью, разрабатывалась уже более века. История началась в 1890-х годах с экспериментальной работы Уильяма Б. Коли, который вводил неактивные бактерии в раковые опухоли, добиваясь ремиссии у некоторых пациентов. Однако только за последние 40 лет в иммунотерапии, особенно в лечении рака, был достигнут серьезный прогресс. В 1970-х годах были разработаны методы лечения антителами, а в 1991 году исследователи создали первую противораковую вакцину, которая была одобрена FDA в 2010 году. За последнее десятилетие иммуноонкология стала одним из самых революционных методов лечения рака.
За последнее десятилетие иммуноонкология стала одним из самых революционных методов лечения рака.Искусственный интеллект (21 век)
Постепенно развиваясь с начала века, искусственный интеллект уже создал впечатляющие технологии, которые значительно изменили ландшафт здравоохранения. Медико-биологические компании и исследовательские институты объединяются с передовыми технологическими гигантами, такими как Google, IBM и Apple, чтобы изобретать более умные и быстрые способы борьбы с болезнями.Эти инновационные технологии варьируются от диагностических инструментов, которые могут обнаруживать злокачественные опухоли, невидимые невооруженным глазом, до систем когнитивных вычислений, которые создают индивидуальные планы лечения для больных раком. Потенциал искусственного интеллекта в обнаружении, диагностике и лечении заболеваний быстро раскрывается перед нами и, похоже, изменит будущее.10 важнейших медицинских открытий 2018 года
Новые исследования мужских противозачаточных средств показали многообещающие результаты.
 Таблетку принимают каждый день в одно и то же время.Image Point Fr / Shutterstock
Таблетку принимают каждый день в одно и то же время.Image Point Fr / Shutterstock В марте исследователи Вашингтонского университета в Сиэтле объявили об успехе испытания противозачаточных таблеток для мужчин.
Рассматриваемая таблетка, называемая диметандролона ундеканоат или DMAU, действует аналогично женскому контроль рождаемости путем сочетания мужского гормона, такого как тестостерон, и прогестина.Прием таблеток один раз в день оказался безопасным — несмотря на увеличение веса пациента и снижение уровня ЛПВП («хорошего») холестерина — остановило производство спермы и снизило выработку тестостерона.
«Эти многообещающие результаты являются беспрецедентными при разработке прототипа мужской таблетки», — заявила Стефани Пейдж, доктор медицинских наук, профессор медицины Вашингтонского университета.
Подробнее: Противозачаточные таблетки для мужчин, резко снижающие уровень тестостерона, проходят трехмесячное испытание.
Это был не единственный прорыв в области контроля над рождаемостью для мужчин. В декабре Gizmodo сообщил, что ученые начали крупное клиническое испытание для проверки мужских гелевых противозачаточных средств.
В декабре Gizmodo сообщил, что ученые начали крупное клиническое испытание для проверки мужских гелевых противозачаточных средств.
Гель, наносимый на спину и плечи один раз в день, содержит комбинацию прогестинового соединения и тестостерона, который всасывается через кожу.
Несмотря на то, что это огромный шаг в плане медицинских достижений, некоторые выразили разочарование тем, что это более удобно, чем некоторые современные способы контроля рождаемости для женщин.
10 революционных моментов в медицине
Вот простой вопрос, на который стоит задуматься, но на который нелегко ответить: какие медицинские достижения за последние 100 лет оказали наибольшее влияние? И если бы вы затем задали этот вопрос некоторым ведущим врачам и ведущим интеллектуалам мира, как бы они ответили? Что они скажут в ответ на то, что хранит бесчисленные миллионы жизней?
К счастью, это не риторическое упражнение. Буквально в прошлом году Совет медицинских исследований в Лондоне, инициатива по финансированию исследований с глобальным охватом, задал именно этот вопрос этим людям. Многие из результатов опроса представлены на следующих страницах вместе с другими открытиями, столь важными на протяжении веков, что они изменили саму суть медицинской практики.
Буквально в прошлом году Совет медицинских исследований в Лондоне, инициатива по финансированию исследований с глобальным охватом, задал именно этот вопрос этим людям. Многие из результатов опроса представлены на следующих страницах вместе с другими открытиями, столь важными на протяжении веков, что они изменили саму суть медицинской практики.
Антибиотики и их непредсказуемое влияние
Когда Совет медицинских исследований проводил свой обзор достижений медицины наибольшего значения, наибольшее количество откликов было за открытие антибиотиков Александром Флемингом.«Без антибиотиков современная медицина в том виде, в каком мы ее знаем, была бы неузнаваема», — написал Стивен Уайтхед, исполнительный директор Ассоциации британской фармацевтической промышленности.
Драматическое заявление о драматическом открытии, которое обязано своим существованием явно недраматическому факту, что Флеминг был неряхой. В 1928 году Флеминг исследовал свойства хорошо известной бактерии Staphylococcus, которая продолжает преследовать нас сегодня в виде MRSA, устойчивой к антибиотикам супербактерии.
Однажды сентябрьским утром он вошел в свою грязную лабораторию, чтобы приступить к работе, и заметил, что одна из его культур стафилококка заросла грибком. Обычно для этого не потребовалось бы ничего, кроме как выбросить чашку Петри.
Но этот гриб был другим. Он был из рода Penicillium, и все колонии стафилококка рядом с ним погибли, в то время как более удаленные были нормальными. Сначала он назвал убивающее бактерии вещество, которое выделяет плесень, прежде чем, наконец, остановился на более формальном названии пенициллина.
После определения способности пенициллина убивать многие виды грамположительных бактерий — например, вызывающих скарлатину, менингит, дифтерию и бактериальную пневмонию — Флеминг отказался от большей части своей работы с новым препаратом из-за трудностей с производством большого количества Это. Примерно 10 лет спустя работа по массовому производству пенициллина выпала на долю двух оксфордских исследователей: Ховарда Флори и Эрнста Чейна.
Итак, хотя Флеминг продолжает получать львиную долю признания в отношении пенициллина, все три исследователя фактически получили Нобелевскую премию по медицине 1945 года. Флори и Чейн ушли в историческую анонимность, а репутация Флеминга продолжает жить. То же самое и с его оригинальной лабораторией, которая была превращена в музей в Лондоне.
Флори и Чейн ушли в историческую анонимность, а репутация Флеминга продолжает жить. То же самое и с его оригинальной лабораторией, которая была превращена в музей в Лондоне.
Все еще довольно грязно.
Применение теории микробов, меняющее мир
Это особенность, что большинство людей сегодня знают имя Lister только по этикетке жидкости для полоскания рта, вызывающей слезы. Это потеря исторического значения наравне с тем, что Эйнштейн в будущем станет не чем иным, как названием франшизы с рогаликами.
Хотя теория микробов — понимание того, что микроорганизмы вызывают множество заболеваний — была впервые предложена в 16 веке и отточена работами Луи Пастера 300 лет спустя, только сэр Джозеф Листер фактически начал применять эти знания в 1860-х годах. медицина из-за этого изменилась к лучшему.
Листер был хирургом в Шотландии в то время, когда большинство его сверстников считали символом статуса носить немытые руки и окровавленные халаты, когда они переходили от операции к операции. Листер, который был знаком с работами Пастера и других, установил связь между отсутствием санитарии и «палатой лихорадкой», высоким уровнем инфицирования пациентов и смертностью, не связанной с предыдущими операциями.
Листер, который был знаком с работами Пастера и других, установил связь между отсутствием санитарии и «палатой лихорадкой», высоким уровнем инфицирования пациентов и смертностью, не связанной с предыдущими операциями.
Пытаясь контролировать инфекции, он первым ввел стерильные процедуры, которые сегодня являются нормой. Он менял халаты и перчатки и тщательно мыл руки между пациентами. Он также стерилизовал хирургические инструменты и операционные с помощью «ослиного двигателя» (подобного показанному на рисунке) для распыления на все мелкого тумана карболовой кислоты, известного дезинфицирующего средства.
Многие другие хирурги высмеивали Листера — до тех пор, пока количество инфекций и лихорадок в отделениях не упало после его операций.
В наши дни опасность внутрибольничных инфекций хорошо известна, и больницы и другие поставщики медицинских услуг, которые не соблюдают санитарные процедуры, привлекаются к ответственности посредством регулятивных действий и судебных исков. Все из-за ренегата шотландского хирурга, чей вклад в медицину спас многие миллионы жизней.
Все из-за ренегата шотландского хирурга, чей вклад в медицину спас многие миллионы жизней.
Профилактика, а не лечение
Со времен Галена и Гиппократа целью медицины было исцеление больных.Хотя это остается самым благородным делом, британский врач Эдвард Дженнер думал, что медицина может быть чем-то большим. Что, если, как он предположил, можно было вообще предотвратить заболевание людей?
Эта идея прижилась в 1796 году, когда он заметил нечто необычное в доярках. Те, кто работал в тесном сотрудничестве с коровами и заразились болезнью, называемой коровьей оспой, не заразились ужасом, которым была натуральная оспа. Исключительно заразная оспа унесла жизни сотен миллионов или даже миллиардов людей с доисторических времен, иногда вызывая крах целых цивилизаций.
Коровья оспа, напротив, вызвала многие из тех же симптомов, что и натуральная оспа, но они были менее тяжелыми по своей природе, и болезнь не была смертельной. Итак, Дженнингс попробовал кое-что, что могло бы изменить историю: он выпил немного гноя из активных волдырей коровьей оспы у доярки и убедил фермера позволить ему ввести гной в руку сына фермера.
Затем, сделав шаг, из-за которого он на всю жизнь был исключен из любой современной медицинской ассоциации, Дженнер ввел мальчику гной оспы. Мальчик легко заболел, но оспа не заболела, и полностью выздоровел через несколько дней.
Так родилась вакцина против оспы и кампания вакцинации, продолжавшаяся до тех пор, пока Всемирная организация здравоохранения не объявила, что болезнь — одно из величайших бедствий человечества — искоренена к 1980 году. , вакцинация, иначе известная как иммунология. С момента открытия Дженнера вакцины были разработаны для многих других болезней. Назовем несколько: корь, краснуха, дифтерия, эпидемический паротит, полиомиелит, менингит, гепатит А и В, грипп, бешенство, желтая лихорадка и столбняк.
Влияние иммунологии на человечество неизмеримо — почти. В начале 2014 года Центры по контролю и профилактике заболеваний немного подсчитали это количество. Было подсчитано, что вакцины, введенные американским младенцам и детям за последние 20 лет, предотвратят 322 миллиона заболеваний, 21 миллион госпитализаций и 732 000 смертей в течение этих жизней.
Большое исследование данных раскрывает эпидемиологию — и выгребную яму
Медицина может быть настолько сильной: безумие скорой помощи при спасении жертвы травмы.Гул и лязг МРТ, вызывающие клаустрофобию. Триумфальная пятерка хирургов после сложной операции.
Некоторые аспекты медицины гораздо мягче в разговоре и разговоре, но не менее важны. Такова эпидемиология — использование наблюдений и статистики для выявления закономерностей, причин, источников и последствий заболеваний среди населения. Это область, сродни бухгалтерскому учету и актуарной науке — больше в Ernst & Young, чем в Young Dr. Kildare.
Но в том-то и дело: эпидемиология находит силу в цифрах.Эта медицинская специальность возникла во время вспышки холеры в Лондоне в 1854 году. Джон Сноу, врач и один из первых защитников спорной тогда теории микробов, подозревал, что болезнь распространяется через загрязненную воду.
Сноу исследовал источник вспышки, опросив местных жителей, чтобы определить обстоятельства жизни жертв холеры. Затем он сделал что-то важное. Он разметил карту с местонахождением всех погибших и нашел общий водяной насос в центре скопления жертв.Другие, которые жили за пределами кластера, пили из того же насоса, когда проезжали через этот район.
Затем он сделал что-то важное. Он разметил карту с местонахождением всех погибших и нашел общий водяной насос в центре скопления жертв.Другие, которые жили за пределами кластера, пили из того же насоса, когда проезжали через этот район.
Когда городские власти сняли ручку с насоса, который был выкопан рядом со старой выгребной ямой, вспышка болезни прекратилась.
Несмотря на то, что в свое время он не был признан, Сноу считается отцом эпидемиологии современных детективов, и его работа сильно повлияла на общественную санитарию и другие меры общественного здравоохранения, принятые во всем мире.
Уродливое лицо войны ведет к современной пластической хирургии
Пластическая хирургия может вызывать в воображении образы голливудских звездочек и их увеличенных и улучшенных тел, но она была разработана и усовершенствована по гораздо менее косметическим причинам.Во время Второй мировой войны количество самолетов и их экипажей было беспрецедентным. Также беспрецедентными были ужасные ожоги, которые получили многие члены экипажа, когда их самолеты были сбиты, что привело к воспламенению топлива.
Арчибальд МакИндо, врач из Новой Зеландии, был среди тех, кому было поручено вылечить этих мужчин. В 1938 году он был назначен пластическим хирургом-консультантом в Королевских военно-воздушных силах, одним из четырех начинающих специалистов в Британии.
В то время медицинская конвенция заключалась в том, чтобы лечить ожог ожогом.Кислота была применена для удаления поврежденной кожи с последующим двухмесячным периодом ожидания, чтобы позволить области достаточно зажить, чтобы перенести операцию. Неудивительно, что для этих пациентов это были восемь недель агонии. Это также оставило у жертв ожогов настолько серьезные шрамы, что они часто избегали публичных выходов на всю оставшуюся жизнь.
Для МакИндоу такие радикальные раны потребовали радикального отхода от условностей. Первым новым методом, который он разработал, была солевая ванна для экипажа, получившего обширные ожоги.Идея этого возникла у пилотов, которые бросили воду в море и, следовательно, оказались в соленой воде. Их ожоги зажили заметно лучше, чем у тех, кто спасался на суше.
Их ожоги зажили заметно лучше, чем у тех, кто спасался на суше.
Следующим шагом для МакИндо было немедленное выполнение операции, рассечение поврежденной ткани и разработка новой техники пересадки кожи для ее замены, также незамедлительно. Это не только уменьшило количество рубцов у пациентов, но и позволило им начать использовать обожженную область гораздо раньше в процессе заживления.
Помимо своего хирургического мастерства, МакИндо также стал очень любим за его понимание психологического воздействия ожогов.Он прекратил одевать пациентов в халаты для выздоравливающих и вместо этого настаивал на том, чтобы им было разрешено носить их обычную военную форму. Он также набирал на работу местные семьи и заставлял их приглашать пациентов на обеды и другие встречи, что помогало его пациентам реинтегрироваться в общество, а не прятаться от него.
Его пациенты быстро окрестили себя «Клубом морских свинок», как ласковое и насмешливое признание того, как новаторские методы МакИндо помогли им. В 1947 году он получил рыцарское звание за свою работу по исцелению тел и психики своих пациентов во время войны. И его методы, в том числе изобретенный им кожный трансплантат, до сих пор используются в реконструктивных операциях.
В 1947 году он получил рыцарское звание за свою работу по исцелению тел и психики своих пациентов во время войны. И его методы, в том числе изобретенный им кожный трансплантат, до сих пор используются в реконструктивных операциях.
Как заставить переливание крови работать, наконец
Достаточно прочитать книгу, действие которой происходит в 1800-х годах или ранее, чтобы знать, что на протяжении истории женщины часто умирали при родах. Одна из наиболее частых причин — неконтролируемое кровотечение после родов.
Джеймс Бланделл, британский акушер, знал, что переливание крови этим женщинам может спасти их.Он также знал, что другие экспериментировали с переливаниями почти 200 лет, часто с фатальными результатами, в основном из-за практики использования крови животных.
После успешных экспериментов по переливанию крови от одного животного одного вида к другому, Бланделл в 1818 году предпринял свою первую человеческую попытку на женщине, у которой было кровотечение после родов. Вместе с ее мужем в качестве донора он перелил женщине 4 унции крови.
Вместе с ее мужем в качестве донора он перелил женщине 4 унции крови.
Она выжила, но не всем последующим пациентам Бланделла повезло.Хотя Бланделл был первым, кто понял, что человеческая кровь должна использоваться на других людях, никто еще не знал, что кровь бывает разных типов — и что переливание крови неправильного типа приведет к иммунному отторжению и, часто, к смерти.
Переливание крови оставалось рискованным делом до 1901 года, когда австрийский врач Карл Ландштайнер обнаружил разные группы крови, и какие из них можно было безопасно смешивать с другими.
Продолжение исследований, проводимых другими специалистами, дало врачам возможность хранить кровь, разделять ее на такие компоненты, как плазма, и проверять на патогены, передающиеся с кровью.Сегодня в США ежегодно проводится около 15 миллионов переливаний.
Конец истерии и наступление женского здоровья
«Ты истеричка!» Забавные штуки, да? Ну, не в викторианскую эпоху.
Женская истерия была широко используемым медицинским диагнозом, особенно в 1800-х и начале 1900-х годов, хотя этот термин приписывают Гиппократу, который основал его на древнегреческом слове «матка» (истерон) в V веке до нашей эры.
Истерия приобрела множество значений на протяжении веков, и к моменту ее исчезновения в качестве медицинского диагноза она служила уловом для всего, что врачи-мужчины (а почти все они были врачами-мужчинами) не понимали о своих пациентах-женщинах. .
Симптомы истерии были, ну, что угодно. Некоторые примеры: обмороки, нытье, раздражительность, сексуальная неудовлетворенность, потеря аппетита, бессонница, лень и потеря речи, но, как ни странно, не пения.
В 20 веке диагноз стал подвергаться более тщательному изучению. Неудивительно, что он не выдержал такой проверки. В конце концов, от него отказались как от диагноза, так как он был удален из DSM-III 1980 года, третьего издания Диагностического и статистического руководства по психическим расстройствам, широко принятого в мире медицинского метода классификации психических расстройств.
Упадок истерии случайно совпал с повышением здоровья женщин как отдельной области медицины. На протяжении 1960-х и 1970-х годов все больше и больше женщин приходили в сферу медицины, до такой степени, что новоиспеченные врачи теперь почти поровну разделены по полу. В период с начала 1900-х до начала 2000-х годов доля женщин, окончивших ординатуру по акушерству и гинекологии, выросла с нуля до примерно 80 процентов. А в 1991 году Министерство здравоохранения и социальных служб США учредило Управление по охране здоровья женщин.
В период с начала 1900-х до начала 2000-х годов доля женщин, окончивших ординатуру по акушерству и гинекологии, выросла с нуля до примерно 80 процентов. А в 1991 году Министерство здравоохранения и социальных служб США учредило Управление по охране здоровья женщин.
Неплохой список достижений для пола, который когда-то считался полностью выведенным из строя истерией.
Где есть дым …
Большинство историй связи между курением табака и раком легких приписывают открытие британскому врачу Ричарду Доллу, сделавшему это заявление в 1950 году во время эпидемии рака легких в послевоенном Соединенном Королевстве.
Хотя он недвусмысленно доказал эту связь, начав в 1951 году 50-летнее продольное исследование, которое показало, что половина курильщиков умерла от своей зависимости, и что отказ от курения был замечательно эффективен в снижении или устранении этого риска, на самом деле он не был первым, кто заметил ссылка на сайт.
Немецкий врач Фриц Ликинт опубликовал статью 1929 года, в которой было показано, что пациенты с раком легких также в подавляющем большинстве курили.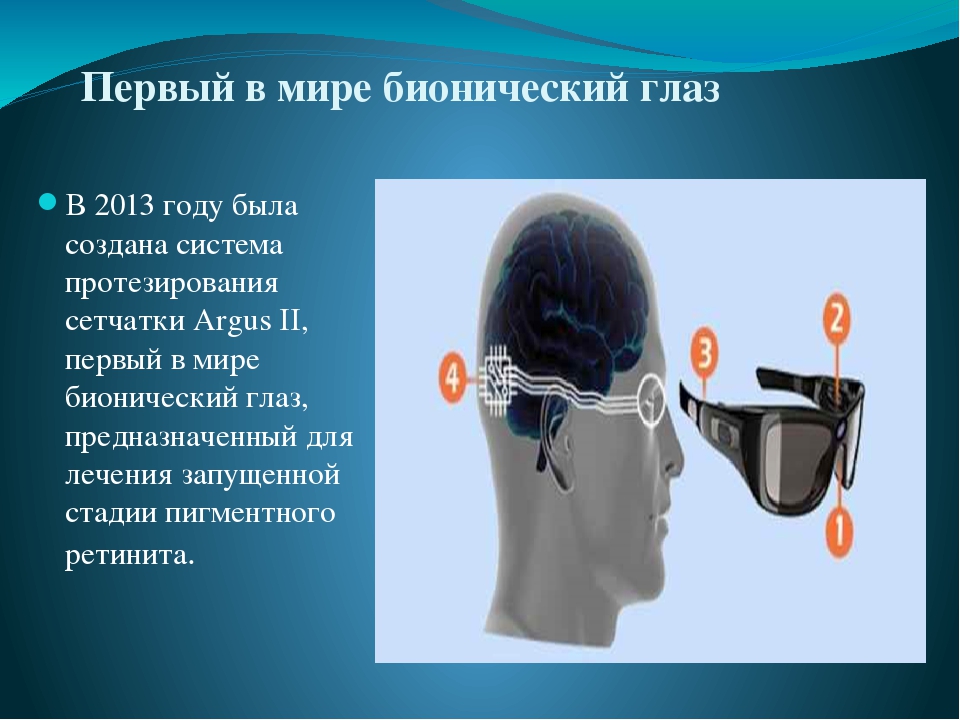 Но поскольку это исследование появилось во время беспорядков в Германии, предшествовавших Второй мировой войне, в течение многих лет оно оставалось незамеченным, если не игнорируемым, вкладом в медицину.
Но поскольку это исследование появилось во время беспорядков в Германии, предшествовавших Второй мировой войне, в течение многих лет оно оставалось незамеченным, если не игнорируемым, вкладом в медицину.
Не то чтобы это имело значение. Перед лицом мощной табачной промышленности и связанного с ней лобби генеральному хирургу США потребовалось до 1964 года, чтобы опубликовать свой первый доклад, в котором американцы узнали о невероятно токсичных последствиях курения, в том числе о том, что курение является основной причиной рака легких.
Тем временем табачная промышленность была занята продвижением пользы для здоровья своей продукции. «Все больше врачей курят верблюдов», — гласило объявление 1946 года. «Покурите удачу, чтобы почувствовать себя на высоте!» сказал другой, из рекламы Lucky Strike 1949 года с 17-летней девушкой в качестве модели.
Сигареты улучшают пищеварение, сохраняют стройную фигуру и создают сложный образ во всех отношениях. Некоторое время Уинстон спонсировал даже телешоу «Флинтстоуны». Каждый эпизод заканчивался тем, что Фред и Вильма вместе зажигали дым, чтобы показать, что Уинстон «такой же вкусный, как и сигарета», даже в каменном веке. Именно в такой обстановке был опубликован отчет главного хирурга 1964 года. Он был разослан в средства массовой информации в субботу, чтобы минимизировать влияние на фондовые рынки и максимизировать освещение в воскресных газетах.
Каждый эпизод заканчивался тем, что Фред и Вильма вместе зажигали дым, чтобы показать, что Уинстон «такой же вкусный, как и сигарета», даже в каменном веке. Именно в такой обстановке был опубликован отчет главного хирурга 1964 года. Он был разослан в средства массовой информации в субботу, чтобы минимизировать влияние на фондовые рынки и максимизировать освещение в воскресных газетах.
Тогдашний генеральный хирург Лютер Терри сказал, что отчет «поразил страну, как бомба». Но это сработало.Опрос, проведенный институтом Гэллапа в 1958 году, показал, что только 44 процента американцев полагали, что курение может вызвать рак; к 1968 году другой опрос Gallup показал, что это число составляет 78 процентов.
В январе 2014 года Журнал Американской медицинской ассоциации отметил 50-летие этого отчета, опубликовав трезвую статистику: с момента публикации отчета 1964 года благодаря усилиям по борьбе с курением было спасено более 8 миллионов жизней американцев.
Мы прошли долгий путь, детка.
От измельчения органов до их трансплантации
Нигде взаимосвязанный характер медицинских достижений не проявляется так ярко, как в области трансплантации органов.Когда врачи начали понимать, как поступает кровь разных типов, они также начали понимать природу иммунного отторжения и то, что делало доноров несовместимыми с их реципиентами.
Врач, которому эти знания очень пригодились, был Джозеф Мюррей, американский врач, который, как и Арчибальд МакИндоу (см. «Уродливое лицо войны ведет к современной пластической хирургии», стр. 76), служил пластическим хирургом во время Второй мировой войны. . Мюррей получил дополнительный опыт в области отторжения тканей, пытаясь пересадить кожу умерших доноров на сильно обожженные участки своих пациентов.
После войны Мюррей сосредоточился на подавлении или предотвращении иммунного ответа, вызывающего отторжение тканей. Если бы Мюррей смог решить эту проблему, врачи могли бы начать выяснять долгожданную способность трансплантировать органы.
Украинский хирург попытался пересадить трупную почку пациенту с почечной недостаточностью в 1930-х годах, в результате чего после операции остались два трупа. Когда в 1954 году Мюррей предпринял следующую попытку медицины пересадить почку, он сделал это, взяв здоровую почку у идентичного — и живого — брата-близнеца своего пациента.Поскольку иммунная система не отторгала генетически идентичную почку, оба брата пережили операцию (показанную выше) и полностью выздоровели.
Затем Мюррей переориентировал свое время на помощь в поиске лекарств, которые подавили бы иммунный ответ в достаточной степени, чтобы сделать возможной трансплантацию между менее совместимыми донорами и реципиентами. Под его руководством другие специалисты в области иммунодепрессантов вскоре разработали такие агенты, как имуран, азатиоприн и преднизон, что позволило Мюррею провести первую трансплантацию почки от неродственного донора в 1959 году.
Мюррей получил Нобелевскую премию по медицине в 1990 году за свои работы в области трансплантации органов и клеток. В 2012 году он перенес инсульт дома в возрасте 93 лет. Мюррей умер в Бригаме и женской больнице, там же, где он провел свою первую операцию по пересадке органов.
В 2012 году он перенес инсульт дома в возрасте 93 лет. Мюррей умер в Бригаме и женской больнице, там же, где он провел свою первую операцию по пересадке органов.
Со времени той первой успешной операции область трансплантации органов расширилась в геометрической прогрессии. Ежегодно в США выполняется около 30 000 трансплантатов, в том числе трансплантаты легких, сердца, печени, поджелудочной железы, кишечника и костей.
Бедлам теперь просто выражение
Скорее всего, вы сказали это: «Чувак, здесь бедлам». Это просто поговорка, правда? Да, и в том-то и дело.
Хотя госпиталь, который когда-то назывался Бедлам — Королевский госпиталь Бетлем в Лондоне — все еще существует, период его истории, когда он получил это прозвище, давно прошел.
Шум, замешательство, визг, плач, бесконечное ношение цепей, необузданное безумие — все это были атрибуты места, где на протяжении сотен лет применялись худшие методы лечения душевнобольных.
Хотя это легко списать на простое отсутствие какого-либо сострадания к психически больным, есть более важный момент: не было никаких хороших вариантов лечения психических заболеваний.
Это начало меняться только в 1950-х годах с разработкой первых антипсихотических препаратов, главным из которых был хлорпромазин, также известный как торазин. Хотя торазин далек от идеального лекарства, он, по крайней мере, дал борющимся врачам эффективный вариант лечения таких психических заболеваний, как шизофрения и маниакальная фаза биполярного расстройства.
Успех торазина в смягчении наихудших форм поведения при таких заболеваниях привел к быстрой и постоянной разработке многих других лекарств от психических заболеваний, включая нейролептики и антидепрессанты. Многие критики считают, что психически больные чрезмерно лечат и демонизируют психоактивные препараты, но немногие захотят вернуться к тем временам, когда эти препараты были доступны.
«Без открытия хлорпромазина мы могли бы все еще иметь жалкие заключения, свидетелями которых были [в то время] отчаянные лекарства», — писал Тревор Тернер, психиатр из больницы Гомертон в Лондоне, в своей номинации препарата как одного из лучших. наиболее значимые медицинские достижения новейшей истории.«Трудно не рассматривать хлорпромазин как своего рода« психический пенициллин »».
наиболее значимые медицинские достижения новейшей истории.«Трудно не рассматривать хлорпромазин как своего рода« психический пенициллин »».
Открытие и разработка лекарств — Центр клинических и трансляционных наук
Открытие и разработка лекарств
Центр клинических и трансляционных исследований Mayo Clinic (CCaTS) предлагает ресурсы, чтобы помочь исследователям в открытии, разработке и тестировании новых терапевтических средств. Эти новые лекарства могут привести к уменьшению симптомов, улучшению качества жизни или, возможно, к обращению вспять трудноизлечимых заболеваний.Эта услуга доступна исследователям во всех кампусах клиники Мэйо.
РесурсCCaTS по открытию и разработке лекарств предполагает сотрудничество с несколькими внешними организациями. Благодаря этому сотрудничеству CCaTS способствует развитию академических и государственно-частных партнерств в процессе открытия, разработки и тестирования лекарств.
Эти сотрудники работают с Mayo Clinic, чтобы предлагать исследователям услуги по открытию и разработке лекарств:
Sanford Burnham Prebys Medical Discovery Institute
Mayo Clinic, через Бюро перевода на практику, сотрудничает с Sanford Burnham Prebys Medical Discovery Institute (Sanford Burnham Prebys) ) для расширения и ускорения разработки новых терапевтических препаратов, нацеленных на множество заболеваний, которые не удовлетворяют медицинские потребности.
Sanford Burnham Prebys финансируется Национальным институтом здравоохранения (NIH) для разработки обширных молекулярных библиотек соединений для эффективных кандидатов в лекарства. Он имеет одну из крупнейших в мире библиотек химических соединений и возможность выполнять роботизированный сверхвысокопроизводительный скрининг, сопоставляя эти соединения с биологическими молекулами.
Сотрудничество с Sanford Burnham Prebys финансируется за счет партнерства между Исследовательским комитетом клиники Майо, CCaTS, Клиническим центром индивидуализированной медицины Майо, онкологическим центром Mayo Clinic и центром регенеративной медицины Mayo Clinic.
Для получения дополнительной информации об этом сотрудничестве прочтите «Клиника Мэйо подключается к открытию новых лекарств» в Discovery’s Edge, онлайн-исследовательском журнале Мэйо.
Предпочтительный статус проекта
Рассмотрите возможность подачи заявки на участие в программе Sanford Burnham Prebys, если вы:
- Определены цели для модуляции
- Имеют или могут разработать скрининговые тесты
- Заинтересованы в идентификации низкомолекулярных соединений
Финансирование
Если вы подаете заявку и были отобраны для участия в этой программе, предоставляется финансирование для сотрудничества с учеными Sanford Burnham Prebys для проверки и оптимизации скринингового анализа, а также для проведения мелкомасштабного скрининга соединений. Вам потребуется доступное финансирование для оплаты любых дополнительных проверок препаратов для раннего скрининга в Mayo. Как только это будет достигнуто, для проведения скрининга лекарств и оптимизации соединений будет изыскиваться финансирование от Национальных институтов здравоохранения (NIH) и из других источников.
Вам потребуется доступное финансирование для оплаты любых дополнительных проверок препаратов для раннего скрининга в Mayo. Как только это будет достигнуто, для проведения скрининга лекарств и оптимизации соединений будет изыскиваться финансирование от Национальных институтов здравоохранения (NIH) и из других источников.
Национальный центр развития трансляционных наук
Национальный центр развития трансляционных наук (NCATS) — это центр NIH с открытой базой данных клинических соединений, доступных для перепрофилирования.Эти соединения не прошли клинические испытания из-за эффективности, но не из-за безопасности. Соединения в базе данных готовы к Фазе I.
Предпочтительный статус проекта
Рассмотрите возможность поиска в базе данных соединений NCATS, если вы определили цель в сигнальном пути, связанном с указанием на заболевание. Вы можете выполнить поиск в базе данных NCATS по имени цели и определить, существует ли соединение для модуляции этой цели. Если вы найдете соединение, которое может модулировать вашу цель, вы можете подать заявку через NCATS для получения доступа к соединению и финансирования для поддержки тестирования фазы I и фазы II.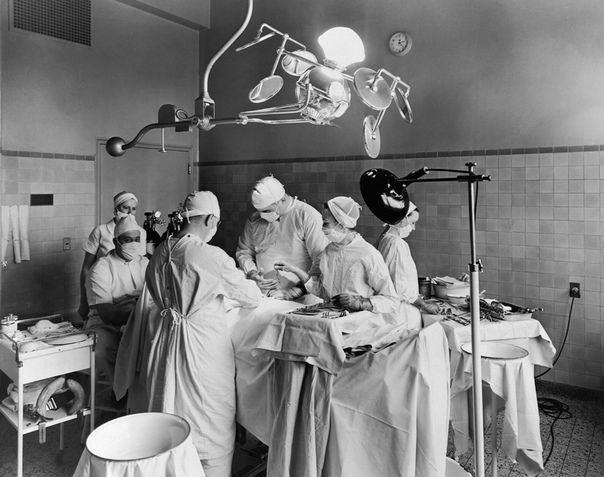
Финансирование
Если вы подаете заявку и выбраны для участия в этой программе, доступ к комплексу и финансирование предоставляется через NCATS.
Услуги по доклинической разработке лекарств
Mayo Clinic Ventures разработала сеть платных внешних исследовательских организаций, которые предоставляют экспертные знания в области разработки лекарственных препаратов, доклинической токсикологии и медицинской химии. Они также могут предложить информацию о взаимодействии с Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов, включая руководство по предварительным заявкам на новые лекарственные препараты и заявки на новые исследуемые лекарства, среди прочего.
Эти ресурсы доступны для каждого проекта. Свяжитесь с Mayo Clinic Ventures для получения дополнительной информации.
Предпочтительный статус проекта
Рассмотрите возможность обращения в Mayo Clinic Ventures за услугами по доклинической разработке лекарств, если вы определили ведущее соединение, низкомолекулярное или биологическое.
Финансирование
У вас должно быть финансирование для оплаты услуг по доклинической разработке лекарств.
Другие возможности
Дополнительные источники финансирования, запросы предложений и другие возможности разработки лекарств также периодически доступны через CCaTS Drug Discovery and Development.
Если у вас есть проект, который вы заинтересованы в реализации с CCaTS, свяжитесь с одним из лиц, перечисленных в разделе «Контакты» ниже.
Дополнительную информацию о возможностях финансирования см. На странице «Возможности финансирования CCaTS».
Контакты
Помимо финансирования и поддержки развития технологий, Бюро перевода в практику (OTP) сотрудничает с несколькими внутренними отделами, такими как Mayo Clinic Ventures и Отдел разработки (необходимо войти в сеть Mayo Clinic), чтобы определить осуществимость продукта.
OTP поддерживает связи с внешними компаниями, занимающимися прототипированием и разработкой, чтобы помочь новаторам Mayo по мере того, как они дорабатывают свои концепции до реализации. Мы заключаем генеральные соглашения об оказании услуг с этими компаниями, что позволяет быстро выполнять их после согласования и подписания технического задания.
Мы заключаем генеральные соглашения об оказании услуг с этими компаниями, что позволяет быстро выполнять их после согласования и подписания технического задания.
.
| Бинты, покрытые лейкопластырем | Пауль Байерсдорф | 1882 |
| Анестетик | Уильям Мортон | 1846 |
| Вакцина против сибирской язвы | Луи Пастер | 1881 |
| Антисептик | Джозеф Листер | 1865 |
| Искусственное сердце | Дентон Кули | 1969 |
| Искусственное бедро | Джон Чарнли | 1972 (усовершенствовано) |
| Искусственная кожа | Доктор.Джон Ф. Берк и Иоаннис Яннас, | 1979 |
| Бактерии (обнаружены) | Антон ван Левенгук | 1674 |
| Противозачаточные таблетки | Грегори Пинкус, Джон Рок и Мин-Чуэ Чанг | 1960 (одобрено FDA) |
| Кровообращение (обнаружено) | Уильям Харви | 1628 (опубликовано) |
| Переливание крови (современное) | Д-р Томас Бланделл | 1818 |
| Вакцина против холеры | Луи Пастер | 1880 |
| Контактные линзы (стекло) | Адольф Фик | 1887 |
| Трансплантация роговицы | Эдуард Зирм | 1905 |
| Лекарства от кашля | Джеймс Смит и сыновья | 1847 |
| Стоматологическая бормашина (с электродвигателем) | Джордж Феллоуз Харрингтон | 1864 |
| Одноразовый шприц | Колин Мердок | 1956 |
| ДНК (структура обнаружена) | Фрэнсис Крик, Джеймс Уотсон, Морис Уилкинс и Розалинда Франклин | 1953 |
| Электрокардиограф | Виллем Эйнтховен | 1903 |
| Противогаз | Гаррет Огастес Морган | 1912 |
| Генетика | Иоганн Грегор Мендель | 1865 |
| Пересадка сердца | Кристиан Барнард | 1967 |
| Шприц для подкожных инъекций | Чарльз Габриэль Праваз и Александр Вуд | 1853 |
| Инсулин (открытие) | Фредерик Бантинг и Чарльз Бест | 1921 |
| Железное легкое | Филип Дринкер | 1929 |
| Микроскоп | Ганс Янсен, его сын Захариас Янсен и Ханс Липперши | 1590 |
| Морфин | Фридрих Вильгельм Адам Сертурнер | 1803 |
| Офтальмоскоп | Чарльз Бэббидж Герман Людвиг фон Гельмгольц | 1847 1851 |
| Кардиостимулятор (человек) | Уилсон Грейтбэтч | 1960 (первое использование) |
| Пастеризация | Луи Пастер | 1864 |
| Патология | Джованни Баттиста Морганьи | 1761 |
| Пенициллин | Александр Флеминг | 1928 |
| Пластическая хирургия | Арчибальд Гектор МакИндо | 1940-е годы |
| Вакцина против полиомиелита | Джонас Солк | 1953 |
| Хинин | Пьер Жозеф Пеллетье и Жозеф Бьенэйме Кавенту | 1820 |
| Вакцина против бешенства | Луи Пастер | 1885 |
| Вакцина против краснухи | Пол Д. Паркман и Гарри М. Мейер младший Паркман и Гарри М. Мейер младший | 1966 |
| Вакцина против цинги | Джеймс Линд | 1753 (опубликовано) |
| Противооспенная вакцина | Эдвард Дженнер | 1796 |
| Стетоскоп | Рене Лаэннек | 1819 |
| Термометр медицинский | Томас Оллбутт | 1866 |
| Рентгеновские лучи | Вильгельм Рентген | 1895 |
Sanford Burnham Prebys Medical Discovery Institute
Онкологический центр Сэнфорда Бернхэма Пребиса, основанный в 1976 году как Фонд исследования рака Ла-Холья, в 1981 году был назначен онкологическим центром базовой лаборатории NCI.Миссия центра — заложить основу для новых методов лечения рака посредством открытий, меняющих парадигму, путем создания, перевода и распространения исключительных фундаментальных научных исследований в области рака. Центр занимается преобразованием современных междисциплинарных фундаментальных исследований в знания о причинах, профилактике и лечении рака, улучшении качества жизни больных раком, а также обучении и обучении следующего поколения ученых-онкологов.
Исследования в онкологическом центре Сэнфорд Бернхэм Пребис
Исследования в онкологическом центре Сэнфорд Бернхэм Пребис основаны на трех программах, отражающих континуум возникновения рака:
- Программа инициации и поддержки опухолей
- Программа «Рак, молекулы и структуры»
- Программа по микросреде опухоли и иммунологии рака
Программы олицетворяют многодисциплинарную культуру сотрудничества центра.
Центр обладает исключительной силой в ранних трансляционных исследованиях, которые включают исследование целей рака и открытие потенциальных терапевтических агентов, посредством ранней доклинической разработки многообещающих методов лечения низкомолекулярными или биологическими агентами.
Избранные научные инициативы в онкологическом центре Сэнфорд Бернхэм Пребис
Как один из семи основных лабораторных онкологических центров NCI, Sanford Burnham Prebys ставит своей целью более быстрое преобразование своих открытий в клинические методы лечения. Ключевые инициативы включают:
Ключевые инициативы включают:
- Объединение с двумя другими онкологическими центрами Сан-Диего (онкологическим центром Мурса в Калифорнийском университете в Сан-Диего и онкологическим центром Солка) для создания Совета онкологических центров Национального института рака Сан-Диего (C3). C3 использует уникальные навыки и ресурсы каждого онкологического центра для ускорения понимания и лечения рака.
- Объединение усилий с клиническими исследователями для создания групп по борьбе с онкологическими заболеваниями, чтобы помочь преобразовать исследовательские инновации в жизнеспособные методы лечения конкретных заболеваний.Команды сосредоточены на проблемных формах рака: остром миелоидном лейкозе, раке головного мозга, груди, легких и поджелудочной железы, и включают в себя врачей из онкологического центра Мурса при Калифорнийском университете в Сан-Диего, детской больницы Рэди в Сан-Диего и онкологического центра Андерсона Скриппса.
- Партнерство с центром Prebys, одним из самых передовых учреждений по открытию лекарств в некоммерческом мире, с целью сократить расстояние между результатами фундаментальных исследований рака и открытием терапевтических средств.

* Этот онкологический центр является одним из семи онкологических центров, которые проводят только лабораторные исследования и не оказывают помощь пациентам.
* Этот профиль предоставлен Медицинским научно-исследовательским институтом Сэнфорд-Бернхэм.
Новости здравоохранения и медицины — ScienceDaily
Исследования делают первые шаги в направлении создания лекарств для лечения распространенного осложнения диабета, гипогликемии
17 декабря 2021 г. — Новое исследование сделало важный шаг к цели по лечению распространенного осложнения диабета — гипогликемии или низкого уровня сахара в крови. Исследователи нашли способ защитить себя…
Прорыв в исследованиях: препараты против ВИЧ, используемые для лечения опухолей головного мозга низкой степени злокачественности
17 декабря 2021 г. — Лекарства, разработанные для лечения СПИДа и ВИЧ, могут дать надежду пациентам, у которых диагностирована наиболее распространенная форма первичной опухоли головного мозга. Это значительный прорыв, потому что, если дальнейшие исследования принесут …
Это значительный прорыв, потому что, если дальнейшие исследования принесут …
Новое исследование проливает свет на то, как ультразвук может быть использован для лечения психических расстройств
17 декабря 2021 г. — Новое исследование показало, как мозг придает значение событиям, а также как транскраниальный ультразвук (ТУЗИ) может нарушить этот процесс.В настоящее время это направление исследований разрабатывается на животных моделях …
Новаторская новая техника для ячеек со штрих-кодом
17 декабря 2021 г. — Ученые разработали новаторский метод более точного и эффективного штрих-кодирования отдельных клеток, который может помочь проложить путь к более быстрому заболеванию …
Рецидив зависимости, вызванный пристрастием к наркотикам, а не только наркотиком
17 декабря 2021 г. — Почему одни люди могут употреблять легкие наркотики контролируемым образом, тогда как другие переключаются на компульсивные, повторяющиеся привычки поиска и употребления наркотиков, которые характерны для употребления психоактивных веществ. ..
..
Новое устройство повышает коммерческую жизнеспособность солнечного топлива
17 декабря 2021 г. — Исследовательская группа разработала новое устройство для искусственного фотосинтеза с замечательной стабильностью и долговечностью, поскольку оно превращает солнечный свет и углекислый газ в два многообещающих источника возобновляемого топлива …
Новое убежище устойчивости к антибиотикам
16 декабря 2021 г. — Гены, которые делают бактерии устойчивыми к антибиотикам, могут сохраняться дольше, чем считалось ранее.Это недавно было показано в новом исследовании, в котором сообщается о ранее неизвестном укрытии для этих …
Конкретные компоненты загрязнения воздуха, признанные более опасными, чем другие
16 декабря 2021 г. — Аммоний является одним из конкретных компонентов мелких твердых частиц (PM2,5), который связан с более высоким риском смерти по сравнению с другими химическими веществами, обнаруженными в нем, согласно новому . ..
..
Стволовые клетки организуются в эмбриоид
Декабрь16, 2021 — Исследователи разработали метод создания комплексов эмбриональных клеток из стволовых клеток мышей. Этот метод позволяет по-новому взглянуть на эмбриональное развитие. В среднесрочной перспективе это может также …
Каннабис может содержать тяжелые металлы и влиять на здоровье потребителей, результаты исследования
16 декабря 2021 г. — В новом метаанализе изучается способность растений каннабиса поглощать тяжелые металлы и обсуждается их влияние на здоровье …
У футболистов колледжа есть нарушения координации и воспаление
Декабрь16 февраля 2021 г. — Спортсмены студенческого футбола с десятилетним или более опытом в спорте имеют связанные с этим нарушения в воспалении, выработке энергии и координации, которые проявляются еще до футбола …
Искусственный интеллект точно предсказывает, у кого разовьется деменция через два года
16 декабря 2021 г. — Искусственный интеллект может предсказать, у каких людей, посещающих клиники памяти, разовьется деменция в течение двух лет с точностью 92%, говорится в новом крупномасштабном исследовании.Используя данные из более …
— Искусственный интеллект может предсказать, у каких людей, посещающих клиники памяти, разовьется деменция в течение двух лет с точностью 92%, говорится в новом крупномасштабном исследовании.Используя данные из более …
Терапевтические наночастицы усиливают иммунотерапию рака
16 декабря 2021 г. — Исследователи обнаружили, что терапевтические наночастицы усиливают иммунотерапию рака и представляют собой возможный новый подход к лечению злокачественного плеврального выпота (ЗПЭ). ПДВ — скопление жидкости …
Новое потенциальное лечение болезни «трансплантат против хозяина» и других воспалительных заболеваний
16 декабря 2021 г. — Исследователи показали, что блокирование цитокинов IL-6 и TNF обеспечивает более эффективный подход к предотвращению опасной для жизни болезни трансплантат против хозяина, воспалительного состояния, которое развивается в…
Вопросы для изучения, широко используемые формулы на основе расы для определения болезни легких
16 декабря 2021 г. — Новые результаты долгосрочного эпидемиологического исследования показывают, что одна из старейших диагностических формул в медицине, основанных на расовой принадлежности, не лучше, чем расовая нейтральность …
— Новые результаты долгосрочного эпидемиологического исследования показывают, что одна из старейших диагностических формул в медицине, основанных на расовой принадлежности, не лучше, чем расовая нейтральность …
Новый способ поиска генетических вариаций устраняет предвзятость при генотипировании человека
16 декабря 2021 г. — С момента первого секвенирования генома человека более 20 лет назад изучение геномов человека основывалось почти исключительно на единственном эталонном геноме, с которым сравниваются другие для идентификации…
COVID-19 мог быстрее распространяться в Соединенных Штатах, потому что первым симптомом был кашель
16 декабря 2021 г. — Штамм вируса COVID-19, который циркулировал в США и Европе во время первой волны пандемии, мог быть особенно заразным, потому что наиболее частым первым симптомом был …
Для СРК особые диеты менее важны, чем ожидалось
16 декабря 2021 г. — Многие люди, страдающие СРК, избегают определенных видов пищи и часто исключают глютен.

